Giải bài tập SGK Hóa 12 Bài 37: Luyện tập: Tính chất hóa học của sắt và hợp chất của sắt
Nội dung hướng dẫn Giải bài tập Hóa 12 Bài 37 dưới đây sẽ giúp các em học sinh nắm vững phương pháp giải bài tập và ôn luyện tốt kiến thức về tính chất hóa học của sắt và hợp chất của sắt Mời các em cùng theo dõi.
Mục lục nội dung

1. Giải bài 1 trang 165 SGK Hóa học 12
Điền công thức hóa học của chất vào những chỗ trống và lập các phương trình hóa học sau:
a) Fe + H2SO4 (đặc) → SO2 + …
b) Fe + HNO3 (đặc) → NO2 + …
c) Fe + HNO3 (loãng) → NO + …
d) FeS2 + HNO3 → NO + Fe2(SO4)3 + …
Phương pháp giải
Dựa vào các chất tham gia (gồm những nguyên tố nào) để viết sản phẩm ( chứa các nguyên tố như ban đầu)
Hướng dẫn giải
Câu a
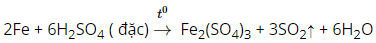
Câu b

Câu c
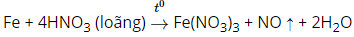
Câu d

2. Giải bài 2 trang 165 SGK Hóa học 12
Bằng phương pháp hóa học, hãy phân biệt ba mẫu hợp kim sau:
Al - Fe; Al - Cu và Cu - Fe.
Phương pháp giải
Dựa vào tính chất hóa học khác nhau giữa các kim loại để chọn thuốc thử phân biệt được các chất.
Hướng dẫn giải
- Lấy mỗi mẫu kim loại 1 lượng nhỏ cho vào dung dịch NaOH, dung dịch không sủi bọt là mẫu Cu-Fe.
- Cho hỗn hợp 2 mẫu còn lại vào HCl, mẫu nào tan hết là Al-Fe, còn lại là Al-Cu.
Phương trình phản ứng:
2Al + 2NaOH + 6H2O → 2Na[Al(OH)4] + 3H2
Fe + 2HCl → FeCl2 + H2
2Al + 6HCl → 2AlCl3 + 3H2
3. Giải bài 3 trang 165 SGK Hóa học 12
Một hỗn hợp gồm Al, Fe, Cu. Hãy trình bày phương pháp hóa học để tách riêng từng kim loại trong hỗn hợp đó. Viết phương trình hóa học của các phản ứng?
Phương pháp giải
Để tìm phương pháp để tách riêng từng kim loại trong hỗn hợp ta dựa vào tính chất hóa học đặc trưng của mỗi kim loại để tách riêng từng kim loại đó.Giải bài 4 trang 165 SGK Hóa học 12
Hướng dẫn giải
Cho dung dịch NaOH dư vào hỗn hợp 3 kim loại thu được hai phần:
- Phần dung dịch là NaAlO2 và NaOH dư
- Phần chất rắn là Cu và Fe
Al + NaOH + H2O → NaAlO2 + 3/2H2
Lấy phần dung dịch dẫn CO2 đến dư thu được kết tủa Al(OH)3. Lọc lấy kết tủa đem nung ngoài không khí đến khối lượng không đổi thu được chất rắn là Al2O3. Điện phân nóng chảy Al2O3 ta được Al.
NaAlO2 + CO2 + H2O → NaHCO3 + Al(OH)3↓
CO2 + NaOH → NaHCO3
CO2 + NaOH → Na2CO3 + H2O
2Al(OH)3 → Al2O3 + 3H2O
2Al2O3 → 4Al + 3O2
Phần chất rắn đem hòa tan trong HCl dư, thu được dung dịch là FeCl2, còn phần chất rắn là Cu. Điện phân dung dịch thu được ta được Fe.
Fe + 2HCl → FeCl2 + H2
FeCl2 → Fe + Cl2
Vậy để tách riêng từng kim loại trong hỗn hợp trên ta dùng NaOH, CO2, HCl, kết hợp phương pháp nung và điện phân dung dịch.
4. Giải bài 4 trang 165 SGK Hóa học 12
Cho một ít bột sắt nguyên chất tác dụng hết với dung dịch H2SO4 loãng thu được 560 ml một chất khí ở đktc. Nếu cho một lượng gấp đôi bột sắt nói trên tác dụng hết với dung dịch CuSO4 thì thu được chất rắn. Tính khối lượng bột sắt đã dùng và khối lượng chất rắn thu được?
Phương pháp giải
Viết phương trình hóa học và dựa vào phương trình để tính toán các đại lượng theo yêu cầu của đề bài.
Hướng dẫn giải
Phương trình hóa học xảy ra:
Fe + H2SO4 → FeSO4 + H2 (1)
Fe + CuSO4 → FeSO4 + Cu (2)
Từ (1) ⇒ nFe (1) = \({n_{{H_2}}} = \frac{{0,56}}{{22,4}} = 0,025\) (mol)
Từ (2) ⇒ nCu (2) = nFe (2) = 2nFe (1) = 0,05 (mol)
Vậy khối lượng Fe đã dùng là: 56.(0,025 + 0,05) = 4,2 (gam) khối lượng chất rắn thu được là 0,05.64 = 3,2 (gam)
5. Giải bài 5 trang 165 SGK Hóa học 12
Biết 2,3 gam hỗn hợp gồm MgO, CuO, FeO tác dụng vừa đủ với 100ml dung dịch H2SO4 0,2M. Khối lượng muối thu được là
A. 3,6 gam.
B. 3,7 gam.
C. 3,8 gam.
D. 3,9 gam.
Phương pháp giải
Để tính khối lượng muối thu được ta thực hiện các bước sau:
- Bước 1: nO(oxit) = nSO42-(muối)
- Bước 2: ⇒ mO = ? ⇒ mkim loại
- Bước 3: mmuối = mkim loại + mSO42-
Hướng dẫn giải
Xét sơ đồ phản ứng:
Hỗn hợp (MgO + FeO+ CuO) + H2SO4 → hỗn hợp muối (MgSO4 + Fe2(SO4)3 + CuSO4) + H2O
Từ sơ đồ trên ta thấy: nO(oxit) = nSO42-(muối) = 0,02 mol
⇒ mO = 16.0,02 = 0,32 (gam); mkim loại = 2,3 – 0,32 = 1,98 (gam)
mmuối = mkim loại + mSO42- = 1,98 + 96.0,02 = 3,9 (gam)
Khối lượng muối thu được là 3,9 gam → Đáp án D.
6. Giải bài 6 trang 165 SGK Hóa học 12
Nguyên tử của nguyên tố X có tổng số hạt proton, nơtron và electron là 82, trong đó số hạt mang điện nhiều hơn số hạt không mang điện là 22. Nguyên tố X là
A. Sắt.
B. Brom.
C. Photpho.
D. Crom.
Phương pháp giải
- Bước 1: Gọi số pronton là p và số notron là n
- Bước 2: Giải hệ 2 ẩn 2 phương trình
2p + n = 82
2p − n = 22
=>p = ? n = ?
- Bước 3: => Tên nguyên tố
Hướng dẫn giải
Tổng số hạt proton, nơtron và electron là 82 ⇒ p + e + n = 82 mà p = e
⇒ Phương trình: 2p + n = 82 (1)
Hạt mang điện (proton điện dương, electron điện âm) nhiều hơn số hạt không mang điện (nơtron) là 22
⇒ 2p - n = 22 (2)
Từ (1) và (2) ta có hệ phương trình:
\(\left\{ \begin{array}{l} 2p + n = 82\\ 2p - n = 22 \end{array} \right. \Rightarrow \left\{ \begin{array}{l} p = 26 = e\\ n = 30 \end{array} \right.\)
Nguyên tố X là sắt
→ Đáp án cần chọn là A.
Tham khảo thêm
- doc Giải bài tập SGK Hóa 12 Bài 31: Sắt
- doc Giải bài tập SGK Hóa 12 Bài 32: Hợp chất của sắt
- doc Giải bài tập SGK Hóa 12 Bài 33: Hợp kim và sắt
- doc Giải bài tập SGK Hóa 12 Bài 34: Crom và hợp chất của crom
- doc Giải bài tập SGK Hóa 12 Bài 35: Đồng và hợp chất của đồng
- doc Giải bài tập SGK Hóa 12 Bài 36: Sơ lược về niken, kẽm, chì, thiếc
- doc Giải bài tập SGK Hóa 12 Bài 38: Luyện tập: TCHH của crom, đồng và hợp chất của chúng
