Hóa học 12 Bài 10: Amino axit
Để biết khái niệm, ứng dụng của amino axit cũng như hiểu những tính chất điển hình của amino axit, eLib xin chia sẻ với các bạn bài 10 amino axit. Nội dung bài đăng bám sát chương trình sách giáo khoa lớp 12. Mời quý thầy cô và các em học sinh cùng tham khảo.
Mục lục nội dung

1. Tóm tắt lý thuyết
1.1. Khái niệm và Danh pháp
a. Khái niệm
Thành phần phân tử: C, H, O, N.
Công thức chung (NH2)xR(COOH)y với
Khái niệm: Amino axit là loại hợp chất hữu cơ tạp chức mà phân tử chứa đồng thời nhóm amino (NH2) và nhóm cacboxyl (COOH).
Ví dụ: CH3-CH(NH2)-COOH (alanine)
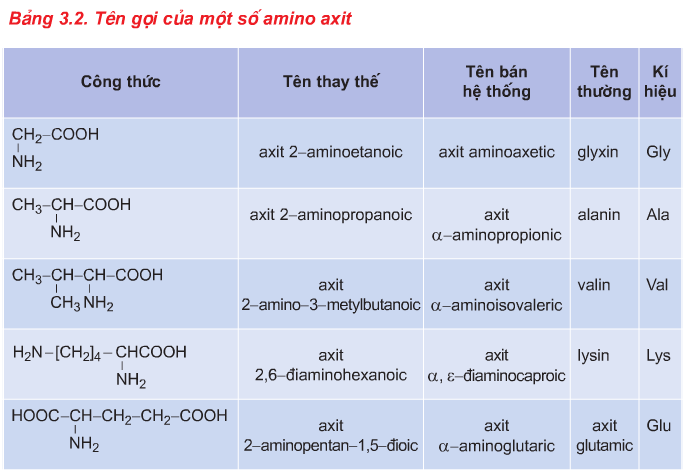
b. Danh pháp
Axit+ số thứ tự C gắn với NH2 + amino + tên gốc axit tương ứng.
1.2. Cấu tạo phân tử
Ở trạng thái kết tinh aa tồn tại ở dạng ion lưỡng cực.
Trong dd dạng ion chuyển một phần nhỏ thành dạng phân tử.
H2N-CH2-COOH ↔ H3N+ – CH2 – COO-
dạng phân tử dạng ion lưỡng cực
1.3. Tính chất hóa học
Tính chất lưỡng tính
Amino axit tác dụng với dd axit vô cơ mạnh và dd bazơ mạnh
H2NCH2COOH + HCl → ClH3NCH2COOH
H3NCH2COOH + HCl → ClNCH2COOH
H2NCH2COOH + NaOH → H2NCH2COONa
Tính axit - bazơ của dung dịch amino axit
Amino axit (NH2)xR(COOH)y
Khi x = y, pHdd 7
H2N-CH2-COOH ↔ H3N+ - CH2-COO-
Glyxin
Khi x < y, pHdd < 7
HOOC-CH2CH2-CH(NH2)-COOH ↔ -OOC-CH2CH2CH(+NH3)-COO- + H+
Axit Glutamic
Khi x > y, pHdd > 7
NH2-[CH2]4-CH(NH2)-COOH ↔ H3N+-[CH2]4CH(+NH3)-COO- + H+
Lysin
Phản ứng riêng của COOH: Phản ứng este hóa
H2NCH2COOH + C2H5OH ↔ H2NCH2COOC2H5 + H2O
Phản ứng trùng ngưng
nH2N-[CH2]5-COOH → (-NH-[CH2]5-CO-)n + nH2O
axit -aminocaproic Policaproamit
1.4. Ứng dụng
Là những hợp chất cơ sở để kiến tạo nên các loại protein trong cơ thể sống.
Muối Mononatri của Axit Glutamic dùng làm bột ngọt, axit glutamic là thuốc bổ trợ thần kinh, methionin là thuốc bổ gan.
Là nguyên liệu để sản xuất nilon 6, nilon 7, ...
2. Bài tập minh họa
2.1. Dạng 1: Bài tập đốt cháy amino axit
Bài 1: Amino axit X chứa một nhóm amin bậc I trong phân tử. Đốt cháy hoàn toàn một lượng X thu được VCO2 : VN2 = 4:1. Công thức cấu tạo của X là:
A. HOOC-CH2CH(NH2)COOH
C. H2NCH2COOH
B. H2NCH2CH2COOH
D. H2NCH2CH2CH2COOH
Hướng dẫn giải
Công thức của aminoaxit X có dạng: H2N – CxHy(COOH)n
Phản ứng: H2N – CxHy(COOH)n → (n + x)CO2 + 1/2 N2
Ta có:
\(\frac{{{n_{C{O_2}}}}}{{{n_{{N_2}}}}} = \frac{4}{1} = \frac{{n + x}}{{\frac{1}{2}}} \to n + x = 2(n \ge 1) \to x = n = 1\)
Vậy X là: H2N – CH2COOH
→ Đáp án C
Bài 2: Đốt cháy hoàn toàn 8,7 g amino axit A (chứa 1 nhóm -COOH) thì thu được 0,3 mol CO2; 0,25mol H2O và 11,2 lít N2 (đktc). Công thức cấu tạo của A là:
A. CH3- CH2 (NH2)-COOH
B. CH3- CH2 (NH2)-COOH
C. CH3 – CH2 – CH2(NH2) - COOH
D. Cả A và B
Hướng dẫn giải
CTPT: CxHyO2Nt , nN2 = 0,05 mol
mO (A) = mA – mC – mH – mN = 8,7 – 0,3.12 – 0,25.2 – 0,05.2.14 = 3,2
⇒ nO(A) = 0,2
A chỉ chứa 1 nhóm -COOH
⇒ nA = nO : 2 = 0,1 mol
nCO2 = x.nA = 0,1x = 0,3 ⇒ x =3
nH2O = (y/2).nA= 0,05y = 0,25 ⇒ y = 5
nN2 = (t/2).nA = 0,05t = 0,05 ⇒ t = 1
⇒ CTPT C3H5O2N
CTCT A: CH3CH2(NH2)-COOH ; H2N- CH2 – CH2 - COOH
→ Đáp án D
2.2. Dạng 2: Dẫn xuất amino axit
Bài 1: Ứng với C3H7NO2 có bao nhiêu đồng phân?
A. 2
B. 3
C. 5
D. 6
Hướng dẫn giải
+ Amino axit: H2N – CH2 – CH2 – COOH; CH3 – CH(NH2) – COOH
+ Este của amino axit: H2N – CH2 – COOCH3
+ Muối: CH2 = CH – COONH4; HCOONH3CH=CH2
+ Hợp chất nitro: CH3 – CH2 – CH2 – NO2
→ Đáp án D
Bài 2: Hợp chất X mạch hở có công thức phân tử C4H9NO2. Cho 10,3 gam X phản ứng vừa đủ với dung dịch NaOH sinh ra khí Y và dung dịch Z. Khí Y nặng hơn không khí và làm giấy quì tím ẩm chuyển thành màu xanh. Dung dịch Z có khả năng làm mất màu nước Brom. Cô cạn Z thu m gam muối khan. Giá trị m là?
A. 10,8
B. 9,4
C. 8,2
D. 9,6
Hướng dẫn giải
X tác dụng NaOH tạo khí Y nên X : R1COOH3NR2
Dung dịch Z làm mất màu nước Brom nên R1 có liên kết đôi C=C, suy ra R1 ≥ 27 (1)
Khí Y làm giấy quỳ tím ẩm hóa xanh nên Y : R2NH2 và MY > 29 → R2 + 16 > 29
⇒ R2 >13 (2)
Ta có : MX = R1 + R2 + 67 = 103 suy ra R1 + R2 = 42 (3)
Từ (1), (2), (3) R1= 27 : CH2=CH- và R2 = 15 : CH3-
CH2=CH-COOH3NCH3 + NaOH → CH2=CH-COONa + CH3NH2 + H2O
0,1mol → 0,1 mol
Giá trị m = 0,1.94 = 9,4 gam
→ Đáp án B
2.3. Dạng 3: Amino axit tác dụng với axit hoặc bazơ
Bài 1: X là một amino axit. Khi cho 0,01 mol X tác dụng với HCl thì dùng hết 80ml dung dịch HCl 0,125M và thu được 1,835g muối khan. Còn khi cho 0,01mol X tác dụng với dung dịch NaOH thì cần dùng 25g dung dịch NaOH 3,2%. Công thức cấu tạo của X là:
A. H2N – C3H6 – COOH
B. H2N – C2H4 – COOH
C. H2N – C3H5(COOH)2
D.(H2N)2C3H5 – COOH
Hướng dẫn giải
nHCl = 0,01 = na.a ⇒ X có 1 nhóm –NH2
nNaOH = 0,02 mol = 2nX ⇒ X có 2 nhóm –COOH
X có dạng: H2N – R – (COOH)2
nmuối = nHCl = 0,01 ⇒ H2N – R – (COONa)2 = 1,835 : 0,01 ⇒ R =41(-C3H5)
→ Đáp án D
Bài 2: Cho 10,3 gam aminoaxit X tác dụng với HCl dư thu được 13,95 gam muối. Mặt khác, cho 10,3 gam amino axit X tác dụng với NaOH (vừa đủ) thu được 12,5 gam muối. Vậy công thức của aminoaxit là:
A. H2N-C3H6-COOH
B. H2N-(CH2)4CH(NH2)-COOH
C. H2N-C2H4-COOH
D. HOOC-(CH2)2-CH(NH2)-COOH
Hướng dẫn giải
X + HCl:
Áp dụng định luật bảo toàn khối lượng: mHCl = mmuối – mX = 3,65
nHCl = n-NH2 =0,1 mol
X + NaOH:
nNaOH = n–COOH = (mmuối – ma.a)/22 = 0,1
n–NH2 = n –COOH ⇒ Dựa vào đáp án amino axit đơn chức chỉ chứa 1 nhóm – COOH và 1 nhóm – NH2
⇒ na.a = nHCl = 0,1 ⇒ MX = 10,3 : 0,1 = 103 ⇒ X là: H2N – C3H6 –COOH
→ Đáp án A
2.4. Dạng 4: Amino axit tác dụng với axit sau đó lẫy hỗn hợp tác dụng với bazơ và ngược lại
Bài 1: Cho amino axit X tác dụng vừa đủ với 16,6 ml dung dịch HCl 20% (d = 1,1 g/ml) thu được muối Y. Y tác dụng vừa đủ với 400 ml dung dịch NaOH 0,5M thu được dung dịch Z. Cô cạn cẩn thận dung dịch Z thu được 15,55 gam muối khan. Công thức của X là:
A. H2N-C2H4-COOH
B. H2N-CH2-COOH
C. H2N-C3H6-COOH
D. H2N-C3H4-COOH
Hướng dẫn giải
nHCl = 0,1 mol; nNaOH = 0,2 mol
⇒ na.a = 0,2 – 0,1 = 0,1
H2N-R-COOH (+ HCl) → ClH3N-R-COOH (+ NaOH) → H2N-R-COONa + NaCl
0,1 0,1 0,1 mol
m (H2N – R – COONa) = 15,55 – 0,1.58,5 = 9,7
M (H2N – R – COONa) = 9,7 : 0,1 = 97
R = 14 (-CH2-)
→ Đáp án A
Bài 2: Cho 0,1 mol amino axit X tác dụng vừa đủ với 100ml NaOH 1M thu được chất hữu cơ Y. Cho Y tác dụng với dung dịch HCl thu được 18,4g muối. Vậy công thức của amino axit X là:
A. H2N – CH2 – CH2 – COOH
B. CH3 – CH(NH2) – COOH
C. H2N – CH2 – COOH
D. HOOC – CH2 – CH2 – CH(NH2) – COOH
Hướng dẫn giải
nNaOH = na.a ⇒ X chỉ chứa 1 nhóm –COOH ( kết hợp với đáp án X chỉ có 1 –NH2)
H2N-R-COOH (+ NaOH) → H2N-R-COONa (+ HCl) → ClH3N-R-COOH + NaCl
0,1 0,1 0,1
Muối gồm: ClH3N – R – COOH (0,1 mol); NaCl (0,1 mol)
⇒ m(ClH3N – R – COOH) = 18,4 – 0,1.58,5 = 12,55
⇒ M (ClH3N – R – COOH) = 12,55 : 0,1 = 125,5
⇒ R = 28 ( - CH2 – CH2 - )
⇒ X là: H2N – CH2 – CH2 – COOH
→ Đáp án A
3. Luyện tập
3.1. Bài tập tự luận
Câu 1: Cho m gam H2NCH2COOH phản ứng hết với dung dịch KOH, thu được dung dịch chứa 16,95 gam muối. Giá trị của m là?
Câu 2: Amino axit X chứa một nhóm -NH2. Cho 15 gam X tác dụng với axit HCl (dư), thu được 22,3 gam muối khan. Công thức cấu tạo thu gọn của X là?
Câu 3: Cho 0,1 mol H2NC3H5(COOH)2 (axit glutamic) vào 125 ml dung dịch HCl 2M, thu được dung dịch X. Cho một lượng vừa đủ dung dịch NaOH vào X để phản ứng xảy ra hoàn toàn số mol NaOH đã phản ứng là?
Câu 4: Cho 7,35 gam axit glutamic phản ứng với 140 ml dung dịch HCl 1M, thu được dung dịch X. Cho 250 ml dung dịch NaOH 1M vào X, thu được dung dịch Y. Cô cạn dung dịch Y, thu được m gam chất rắn khan. Biết các phản ứng xảy ra hoàn toàn, giá trị của m là?
Câu 5: Amino axit X có công thức H2NCxHy(COOH)2. Cho 0,1 mol X vào 0,2 lít dung dịch H2SO4 0,5M, thu được dung dịch Y. Cho Y phản ứng vừa đủ với dung dịch gồm NaOH 1M và KOH 3M, thu được dung dịch chứa 36,7 gam muối. Phần trăm khối lượng của nitơ trong X là?
3.2. Bài tập trắc nghiệm
Câu 1: Amino axit là hợp chất hữu cơ trong phân tử có chứa nhóm chức
A. cacboxyl và hiđroxyl
B. hiđroxyl và amino
C. cacboxyl và amino
D. cacbonyl và amino
Câu 2: Công thức của glyxin là
A. CH3NH2
B. H2NCH(CH3)COOH
C. H2NCH2COOH
D. C2H5NH2
Câu 3: Số nhóm amino và số nhóm cacboxyl có trong một phân tử axit glutamic tương ứng là
A. 2 và 2
B. 1 và 2
C. 2 và 1
D. 1 và 1
Bài 4: Số đồng phân cấu tạo của amino axit ứng với công thức phân tử C3H7O2N là
A. 2
B. 4
C. 3
D. 1
Bài 5: Dung dịch nào sau đây làm quỳ tím đổi thành màu xanh?
A. dung dịch alanin
B. dung dịch glyxin
C. dung dịch lysin
D. dung dịch valin
3.3. Trắc nghiệm Online
Các em hãy luyện tập bài trắc nghiệm Amino axit Hóa học 12 sau để nắm rõ thêm kiến thức bài học.
4. Kết luận
Qua nội dung bài học các em cần nắm các ý chính trọng tâm trong bài như sau:
- Khái niệm, tính chất hóa học điển hình của Amino axit
- Ứng dụng của Amion axit
