Giải bài tập SGK Hóa 10 Nâng cao Bài 33: Luyện tập về clo và hợp chất của clo
Nhằm củng cố và vận dụng đã kiến thức đã học của clo và hợp chất của clo vào bài tập. eLib xin chia sẻ với các em nội dung giải bài tập SGK nâng cao 11 dưới đây. Với nội dung các bài tập có phương pháp giải và hướng dẫn giải chi tiết, hi vọng rằng đây sẽ là tài liệu giúp các em học tập tốt hơn.
Mục lục nội dung

1. Bài 1 trang 136 SGK Hóa 10 nâng cao
Trong các dãy chất dưới đây, dãy nào gồm toàn các chất có thể tác dụng với clo?
A. Na, H2, N2;
B. NaOH(dd), NaBr(dd), NaI(dd);
C. KOH(dd), H2O, KF(dd);
D. Fe, K, O2
Phương pháp giải
Để giải bài tập này cần nắm vững tính chất hóa học của clo
- Tác dụng với kim loại
- Tác dụng với phi kim
- Tác dụng với nước và dung dịch kiềm
- Tác dụng với muối của các halogen khác
- Tác dụng với chất khử khác
- Phản ứng thế, phản ứng cộng, phản ứng phân huỷ với một số hợp chất hữu cơ
Hướng dẫn giải
Chọn B.
Dãy chất tác dụng với clo là:
Cl2 + 2NaOH → NaCl + NaClO + H2O
Cl2 + 2NaBr → 2NaCl + Br2
Cl2 + 2NaI → 2NaCl + I2
2. Bài 2 trang 136 SGK Hóa 10 nâng cao
Viết phương trình hóa học thực hiện các biến hóa:
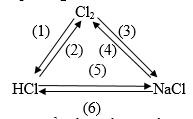
Phương pháp giải
Để giải bài tập này cần nắm vững tính chất hóa học của clo và hợp chất của clo
Hướng dẫn giải
Các phản ứng xảy ra:
(1) C2 + H2 → 2HCl (đk: ánh sáng)
(2) 4HCl + MnO2 → MnCl2 + Cl2 + 2H2O
(3) Cl2 + 2Na → 2NaCl
(4) 2NaCl + 2H2O (đpdd có mn) → 2NaOH + Cl2 + H2
(5) HCl + NaOH → NaCl + H2O
(6) NaCl + H2SO4 đặc → HCl + NaHSO4
3. Bài 3 trang 136 SGK Hóa 10 nâng cao
Người ta có thể điều chế KCl bằng:
1) một phản ứng hóa hợp.
2) một phản ứng phân hủy.
3) một phản ứng trao đổi.
4) một phản ứng thế.
a. Hãy dẫn ra phản ứng cho mỗi trường hợp trên.
b. Trường hợp nào là phản ứng oxi hóa-khử? Trong đó số oxi hóa của nguyên tố clo thay đổi như thế nào?
Phương pháp giải
Để giải bài tập này cần nắm được nguyên tắc điều chế muối clorat
Hướng dẫn giải
Câu a: Các phản ứng điều chế KCl
Một phản ứng hóa hợp:
2K + Cl2 → 2KCl (1)
Một phản ứng phân hủy:
2KClO3 → 2KCl + 3O2 (2) (xt: MnO2, to)
Một phản ứng trao đổi:
K2SO4 + BaCl2 → BaSO4 + 2KCl (3)
Một phản ứng thế:
2K + 2HCl → 2KCl + H2 (4)
Câu b: Các phản ứng (1), (2) và (4) là phản ứng oxi hóa-khử.
Trong (1): Số oxi hóa cửa clo giảm từ 0 xuống - 1.
Trong (2): Số oxi hóa của clo giảm từ +5 xuống -1.
Trong (3) và (4): số oxi hóa của clo không thay đổi.
4. Bài 4 trang 136 SGK Hóa 10 nâng cao
Viết phương trình hóa học của phản ứng thực hiện các biến hóa dưới đây, ghi tên các chất và điều kiện của phản ứng.
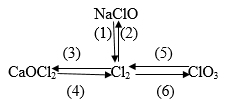
Phương pháp giải
Để giải bài tập này cần nắm vững tính chất hóa học hợp chất của clo
Hướng dẫn giải
Các phản ứng xảy ra :
(1) NaClO + 2HCl → NaCl + Cl2 + H2O
(2) Cl2 + 2NaOH → NaCl + NaClO + H2O
(3) Cl2 + Ca(OH)2 rắn → CaOCl2 + H2O
(4) CaOCl2 + 2HCl → CaCl2 + Cl2 + H2O
(5) KClO3 + 6HC1 → 3Cl2 + KCl + 3 H2O
(6) 3Cl2 + 6KOH → 5KCl + KClO3 + 3H2O
Tên các chất:
- NaClO: Natri hipoclorit;
- CaOCl2: Canxi clorua hipoclorit (clorua vôi)
- KClO3: Kali clorat;
- NaBrO: Natri hipobromit
5. Bài 5 trang 136 SGK Hóa 10 nâng cao
Hỗn hợp khí A gồm clo và oxi. A phản ứng vừa hết với một hỗn hợp gồm 4,8 gam magie và 8,10g nhôm tạo ra 37,05 gam hỗn hợp các muối clorua và oxit của hai kim loại. Xác định thành phần phần trăm theo khối lượng và theo thể tích hỗn hợp A.
Phương pháp giải
- Viết phương trình electron của phản ứng
- Áp dụng bảo toàn electron: ∑ne nhường = ∑e nhận
- Áp dụng bảo toàn khối lượng: mAl + mMg + mO2 + mCl2 = mZ
→ Tìm được a, b → Thành phần phần trăm thể tích → Phần trăm khối lượng mỗi khí
Hướng dẫn giải
nAl = 8,1/27 = 0,3 (mol); nMg = 4,8/24 = 0,2 (mol).
Đặt số mol O2 và Cl2 cần dùng lần lượt là a mol và b mol
Qúa trình nhường electron
Alo - 3e → Al3+
0,3 0,9 0,3
Mgo - 2e → Mg2+
0,2 0,4 0,2
Quá trình nhận electron
O2 + 4e → 2O2-
a 4a 2a
Cl2 + 2e → 2Cl-
b 2b 2b
∑ne nhường = (0,9 + 0,4) = 1,3 (mol)
∑ne nhận = (4a + 2b)(mol)
∑ne nhường = ∑e nhận ⇒ 1,3 = 4a + 2b (∗)
Áp dụng định luật bảo toàn khối lượng ta có:
mAl + mMg + mO2 + mCl2 = mZ
⇒ mO2 + mCl2 = 32a + 71b = 37,05 - ( 8,1 + 4,8) = 24,15 (∗∗)
Giải hệ (∗) và (∗∗) ta được: (a = 0,2; b = 0,25)
Thành phần phần trăm thể tích mỗi khí trong hỗn hợp A
%VO2 = %nO2 = (0,2. 100%)/(0,2 + 0,25) = 44,44%;
%VCl2 = %nCl2 = 100% - 44,44% = 55,56%
Thành phần phần trăm khối lượng mỗi khí trong hỗn hợp A
%mO2/A = (6,4/24,15). 100% = 26,5%;
%mCl2/A = (17,75/24,15). 100% = 73,5%.
6. Bài 6 trang 136 SGK Hóa 10 nâng cao
Muối ăn bị lẫn các tạp chất là Na2SO4, MgCl2, CaCl2 và CaSO4. Hãy trình bày phương pháp hóa học để loại bỏ các tạp chất, thu được NaCl tinh khiết. Viết phương trình hóa học của các phản ứng.
Phương pháp giải
Dùng Na2CO3, BaCl2 và HCl
Hướng dẫn giải
- Cho dung dịch Na2CO3 vừa đủ vào dung dịch muối ăn có lẫn tạp chất Na2SO4, MgCl2, CaCl2, CaSO4 để loại bỏ các ion Mg2+, Ca2+.
Na2CO3 + MgCl2 → MgCO3 + 2NaCl
Na2CO3 + CaCl2 → CaCO3 +2NaCl
Na2CO3 + CaSO4 → CaCO3+ Na2SO4
- Lọc bỏ kết tủa sau đó cho dung dịch BaCl2 vào dung dịch nước lọc để loại bỏ ion SO42-
BaCl2 + Na2SO4 → BaSO4 + 2NaCl
- Lọc bỏ kết tủa BaSO4, cho dung dịch Na2CO3 vào dung dịch nước lọc (nếu còn dư BaCl2) để loại bỏ ion Ba2+.
BaCl2 + Na2CO3 → BaCO3 + 2NaCl
- Lọc bỏ kết tủa BaCO3 , cho dung dịch HCl vào dung dịch nước lọc (nếu còn dư Na2CO3 ) và đun nhẹ được NaCl tinh khiết.
2HCl + Na2CO3 → 2NaCl + H2O + CO2
Tham khảo thêm
- doc Giải bài tập SGK Hóa 10 Nâng cao Bài 29: Khái quát về nhóm halogen
- doc Giải bài tập SGK Hóa 10 Nâng cao Bài 30: Clo
- doc Giải bài tập SGK Hóa 10 Nâng cao Bài 31: Hiđro clorua - Axit clohiđric
- doc Giải bài tập SGK Hóa 10 Nâng cao Bài 32: Hợp chất có oxi của clo
- doc Giải bài tập SGK Hóa 10 Nâng cao Bài 34: Flo
- doc Giải bài tập SGK Hóa 10 Nâng cao Bài 35: Brom
- doc Giải bài tập SGK Hóa 10 Nâng cao Bài 36: Iot
- doc Giải bài tập SGK Hóa 10 Nâng cao Bài 37: Luyện tập Chương 5
