Giải bài tập SGK Hóa 10 Nâng cao Bài 9: Bảng tuần hoàn các nguyên tố hóa học
eLib xin chia sẻ tài liệu Giải bài tập Bảng tuần hoàn các nguyên tố hóa học giúp các bạn học sinh nắm chắc kiến thức của bài học để từ đó có thể vận dụng vào việc giải các bài tập trong SGK Hóa lớp 10 nâng cao trang 39. Hy vọng với tài liệu này sẽ giúp ích cho các bạn học tốt Hóa 9. Mời các bạn cùng tham khảo.
Mục lục nội dung
1. Giải bài 1 trang 39 SGK Hóa học 10 nâng cao
2. Giải bài 2 trang 39 SGK Hóa học 10 nâng cao
3. Giải bài 3 trang 39 SGK Hóa học 10 nâng cao
4. Giải bài 4 trang 39 SGK Hóa học 10 nâng cao
5. Giải bài 5 trang 39 SGK Hóa học 10 nâng cao
6. Giải bài 6 trang 39 SGK Hóa học 10 nâng cao

1. Giải bài 1 trang 39 SGK Hóa 10 nâng cao
Nguyên tử các nguyên tố xếp ở chu kì 6 có số lớp electron trong nguyên tử là:
A. 3.
B. 5.
C. 6.
D. 7.
Chọn đáp án đúng.
Phương pháp giải
Số thứ tự của chu kì trùng với số lớp electron của nguyên tử các nguyên tố trong chu kì đó.
Hướng dẫn giải
Số lớp electron trong nguyên tử ở chu kì 6 là 6 lớp e.
Đáp án C
2. Giải bài 2 trang 39 SGK Hóa 10 nâng cao
Số nguyên tố trong chu kì 3 và chu kì 5 là:
A. 8 và 18.
B. 18 và 8.
C. 8 và 8.
D. 18 và 18.
Chọn đáp án đúng.
Phương pháp giải
Dựa vào bảng tuần hoàn nguyên tố để trả lời câu hỏi
Hướng dẫn giải
Chọn A.
- Số nguyên tố thuộc chu kì 3 gồm: Na (Z = 11) đến Ar (Z = 18)
⇒ Có tất cả 8 nguyên tố.
- Số nguyên tố thuộc chu kì 5 gồm: Rb (Z= 37) đến Xe (Z = 54).
⇒ Có tất cả là 18 nguyên tố.
3. Giải bài 3 trang 39 SGK Hóa 10 nâng cao
Trong bảng tuần hoàn các nguyên tố, số chu kì nhỏ và chu kì lớn là:
A. 3 và 3.
B. 3 và 4.
C. 4 và 4.
D. 4 và 3.
Chọn đáp án đúng.
Phương pháp giải
Số thứ tự của chu kì trùng với số lớp electron của nguyên tử các nguyên tố trong chu kì đó.
* Chu kì nhỏ: gồm chu kì 1, 2, 3.
* Chu kì lớn: gồm chu kì 4, 5, 6, 7.
Hướng dẫn giải
Có tất cả 7 chu kỳ trong đó có 3 chu kỳ nhỏ và 4 chu kỳ lớn
Đáp án B
4. Giải bài 4 trang 39 SGK Hóa 10 nâng cao
Số hiệu nguyên tử của các nguyên tố trong bảng tuần hoàn cho ta biết những thông tin gì?
Phương pháp giải
- Số hiệu nguyên tử Z của một nguyên tố là số đơn vị điện tích hạt nhân của nguyên tố đó.
- Nếu biết số khối A và số hiệu nguyên tử Z của nguyên tố, ta tính được số nơtron trong hạt nhân nguyên tử của nguyên tố đó N = A – Z → Số p, số e
Hướng dẫn giải
Số hiệu nguyên tử cho biết:
- Số thứ tự ô nguyên tố
- Số đơn vị diện tích hạt nhân
- Số proton và số electron.
5. Giải bài 5 trang 39 SGK Hóa 10 nâng cao
Vì sao chu kì 2 và chu kì 3, mỗi chu kì có 8 nguyên tố?
Phương pháp giải
Dựa vào nguyên lí phân bố electron trong nguyên tử để trả lời bài tập
Hướng dẫn giải
Chu kì 2 và chu kì 3, mỗi chu kì có 8 nguyên tố vì theo các nguyên lí và quy tắc phân bố electron trong nguyên tử, có 8 nguyên tố mà nguyên tử có 2 lớp electron và cũng chỉ có 8 nguyên tố mà nguyên tử của chúng có 3 lớp electron.
6. Giải bài 6 trang 39 SGK Hóa 10 nâng cao
a) Nhóm nguyên tố là gì?
b) Các nguyên tố s, p, d, f thuộc những nhóm nào trong bảng tuần hoàn?
Phương pháp giải
- Nhóm nguyên tố là tập hợp các nguyên tố mà nguyên tử có cấu hình electron tương tự nhau, do đó có tính chất hóa học gần giống nhau và được xếp thành một cột.
- Khối các nguyên tố s: gồm các nguyên tố nhóm IA và IIA
- Khối các nguyên tố p: gồm các nguyên tố thuộc các nhóm từ IIIA đến VIIIA (trừ He).
- Khối các nguyên tố d: gồm các nguyên tố thuộc nhóm B.
- Khối các nguyên tố f: gồm các nguyên tố thuộc họ Lantan và họ Actini.
Hướng dẫn giải
Câu a: Nhóm nguyên tố là tập hợp các nguyên tố mà nguyên tử có cấu hình electron tương tự nhau, do đó có tính chất hóa học gần giống nhau và được xếp thành một cột.
Câu b: Các nguyên tố s thuộc nhóm IA, IIA và He thuộc nhóm VIIIA.
Các nguyên tố p thuộc các nhóm IIIA, IVA, VA, VIA, VIIA, VIIIA (trừ He). Các nguyên tô d thuộc các nhóm IB đến VIIIB.
Các nguyên tố f thuộc 2 họ nguyên tố Lantan và Actini.
7. Giải bài 7 trang 39 SGK Hóa 10 nâng cao
Viết cấu hình electron nguyên tử của các nguyên tố từ Z = 1 đến Z = 20.
Phương pháp giải
B1: Điền lần lượt các e vào các phân lớp theo thứ tự tăng dần mức năng lượng.
B2: Sắp xếp lại theo thứ tự các lớp và phân lớp theo nguyên tắc từ trong ra ngoài.
B3: Xem xét phân lớp nào có khả năng đạt đến bão hòa hoặc bán bão hòa thì có sự sắp xếp lại các electron ở các phân lớp (chủ yếu là d và f)
Hướng dẫn giải
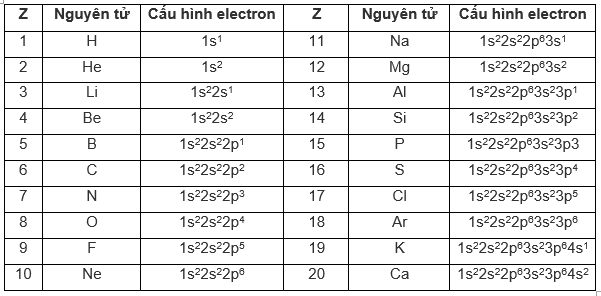
8. Giải bài 8 trang 39 SGK Hóa 10 nâng cao
Viết cấu hình electron nguyên tử của các nguyên tố selen (Z = 34), kripton (Z = 36) và xác định vị trí của chúng trong bảng tuần hoàn.
Phương pháp giải
Viết cấu hình electron theo 3 bước:
- B1: Điền lần lượt các e vào các phân lớp theo thứ tự tăng dần mức năng lượng.
- B2: Sắp xếp lại theo thứ tự các lớp và phân lớp theo nguyên tắc từ trong ra ngoài.
- B3: Xem xét phân lớp nào có khả năng đạt đến bão hòa hoặc bán bão hòa thì có sự sắp xếp lại các electron ở các phân lớp (chủ yếu là d và f)
→ Rút ra nhận xét
Hướng dẫn giải
Cấu hình electron của selen (Z = 34) là:
Se (Z = 34): 1s22s22p63s23p63d104s24p4 Se thuộc ô số 34 nhóm VIA, chu kì 4.
Cấu hình eleetron của kripton (Z = 36) là:
Kr (Z = 36): 1s22s22p63s23p63d104s24p6 Kr thuộc ô số 36 nhóm VIIIA, chu kì 4.
Tham khảo thêm
- doc Giải bài tập SGK Hóa 10 Nâng cao Bài 10: Sự biến đổi tuần hoàn cấu hình electron nguyên tử của các NTHH
- doc Giải bài tập SGK Hóa 10 Nâng cao Bài 11: Sự biến đổi một số đại lượng vật lí của các nguyên tố hóa học
- doc Giải bài tập SGK Hóa 10 Nâng cao Bài 12: Sự biến đổi tính KL, tính phi kim của các NTHH, định luật tuần hoàn
- doc Giải bài tập SGK Hóa 10 Nâng cao Bài 13: Ý nghĩa của bảng tuần hoàn các NTHH
- doc Giải bài tập SGK Hóa 10 Nâng cao Bài 14: Luyện tập chương 2
