Giải bài tập SGK Hóa 9 Bài 2: Một số oxit quan trọng
Hướng dẫn Giải bài tập Hóa học 9 Bài 2 Một số oxit quan trọng dưới đây sẽ giúp các em học sinh nắm vững phương pháp giải bài tập và ôn luyện tốt kiến thức. Mời các em cùng theo dõi.
Mục lục nội dung
1. Giải bài 1 trang 9 SGK Hóa lớp 9
2. Giải bài 2 trang 9 SGK Hóa lớp 9
3. Giải bài 3 trang 9 SGK Hóa lớp 9
4. Giải bài 4 trang 9 SGK Hóa lớp 9
1. Giải bài 1 trang 11 SGK Hóa lớp 9
2. Giải bài 2 trang 11 SGK Hóa lớp 9
3. Giải bài 3 trang 11 SGK Hóa lớp 9
4. Giải bài 4 trang 11 SGK Hóa lớp 9

A. Canxi oxit
1. Giải bài 1 trang 9 SGK Hóa lớp 9
Bằng phương pháp hóa học nào có thể nhận biết được từng chất trong mỗi dãy chất sau?
a) Hai chất rắn màu trắng là CaO và Na2O.
b) Hai chất khí không màu là CO2 và O2.
Viết các phương trình hóa học.
Phương pháp giải
Với bài tập nhận biết, cần nắm các nguyên tắc cơ bản sau:
- Đối với hỗn hợp rắn:
- Cần hòa vào nước để tạo dung dịch.
- Sau đó dựa vào tính chất hóa học đặc trưng và khác nhau của các chất có thể quan sát được, sử dụng phương pháp phù hợp để nhận biết.
- Đối với hỗn hợp khí: Dựa vào tính chất hóa học đặc trưng khác nhau có thể quan sát được của các khí, sục các khí vào các chất thích hợp để nhận biết.
Hướng dẫn giải
Câu a: Nhận biết hai chất rắn màu trắng là CaO và Na2O
- Lấy mỗi chất cho vào mỗi cốc đựng nước, khuấy cho đến khi chất cho vào không tan nữa, sau đó lọc để thu lấy hai dung dịch.
- Dẫn khí CO2 vào mỗi dung dịch:
Nếu ở dung dịch nào xuất hiện kết tủa (làm dung dịch hóa đục) thì đó là dung dịch Ca(OH)2, suy ra cho vào cốc lúc đầu là CaO, nếu không thấy kết tủa xuất hiện chất cho vào cốc lúc đầu là Na2O.
Các phương trình hóa học đã xảy ra:
Na2O + H2O → 2NaOH
CaO + H2O → Ca(OH)2
2NaOH + CO2 → H2O + Na2CO3 (tan trong nước)
Ca(OH)2 + CO2 → H2O + CaCO3 (kết tủa không tan trong nước)
Câu b: Nhận biết hai chất khí không màu là CO2 và O2
- Cách 1: Cho tàn đóm đỏ vào từng khí.Khí nào làm tàn đóm bùng cháy trở lại là khí O2 còn lại là CO2.
- Cách 2: Sục hai chất khí không màu vào hai ống nghiệm chứa nước vôi Ca(OH)2 trong. Ống nghiệm nào bị vẩn đục, thì khí ban đầu là CO2, khí còn lại là O2.
Phương trình hóa học:
Ca(OH)2 + CO2 → H2O + CaCO3
2. Giải bài 2 trang 9 SGK Hóa lớp 9
Hãy nhận biết từng chất trong mỗi nhóm chất sau bằng phương pháp hóa học.
a) CaO, CaCO3
b) CaO, MgO
Viết phương trình hóa học.
Phương pháp giải
Với bài tập nhận biết, cần nắm nguyên tắc cơ bản sau: Dựa vào tính chất hóa học khác nhau của 2 chất để nhận biết được từng chất.
Trong bài này, có thể dùng nước để nhận biết.
Hướng dẫn giải
Câu a: Lấy mỗi chất cho ống nghiệm hoặc cốc chứa sẵn nước
- Ở ống nghiệm nào thấy chất rắn tan và nóng lên, chất cho vào là CaO.
- Ở ống nghiệm nào thấy chất rắn không tan và không nóng lên, chất cho vào là CaCO3.
Phương trình hóa học:
CaO + H2O → Ca(OH)2
Câu b: Lấy mỗi chất cho ống nghiệm hoặc cốc chứa sẵn nước
- Ở ống nghiệm nào thấy chất rắn tan và nóng lên, chất cho vào là CaO.
- Ở ống nghiệm nào thấy chất rắn không tan và không nóng lên, chất cho vào là MgO.
Phương trình hóa học:
CaO + H2O → Ca(OH)2
3. Giải bài 3 trang 9 SGK Hóa lớp 9
200ml dung dịch HCl có nồng độ 3,5M hòa tan vừa hết 20 g hỗn hợp hai oxit CuO và Fe2O3
a) Viết các phương trình hóa học.
b) Tính khối lượng của mỗi oxit có trong hỗn hợp ban đầu.
Phương pháp giải
Với dạng toán hỗn hợp kim loại tác dụng với axit, ta thực hiện các bước sau:
- Bước 1: Đổi số mol của HCl, gọi số mol của CuO và lần lượt là x, y.
- Bước 2: Viết phương trình hóa học, tính số mol HCl theo x và y.
CuO + 2HCl → CuCl2 + H2O
x → 2x x
Fe2O3 + 6HCl → 2FeCl3 + 3H2O
y → 6y 2y
- Bước 3: Giải hệ 2 ẩn 2 phương trình theo khối lượng của oxit và số mol HCl.
- Bước 4: Tính khối lượng của mỗi oxit theo x, y vừa tìm được.
Hướng dẫn giải
Câu a: Phương trình hóa học của phản ứng
CuO + 2HCl → CuCl2 + H2O
Fe2O3 + 6HCl → 2FeCl3 + 3H2O
Câu b: Khối lượng của mỗi oxit có trong hỗn hợp ban đầu
\({n_{HCl}} = \frac{{3,5.200}}{{1000}} = 0,7\;mol\)
Gọi x, y là số mol của CuO và Fe2O3
Ta có nHCl = 2x + 6y = 0,7 (1)
mCuO + mFe2O3 = 80x + 160y = 20 (2)
Từ (1) và (2) ta có hệ phương trình:
\(\left\{ {\begin{array}{*{20}{l}}
{2x + 6y = 0,7} \\
{80x + 160y = 20}
\end{array}} \right. \Rightarrow \left\{ {\begin{array}{*{20}{l}}
{x = 0,05(mol)} \\
{y = 0,1(mol)}
\end{array}} \right.\)
Khối lượng của mỗi oxit có trong hỗn hợp ban đầu là:
mCuO = 0,05.80 = 4 (g).
mFe2O3 = 0,1.160 = 16 (g).
4. Giải bài 4 trang 9 SGK Hóa lớp 9
Biết 2,24 lít khí CO2 (đktc) tác dụng vừa hết với 200 ml dung dịch Ba(OH)2 sản phẩm là BaCO3 và H2O
a) Viết phương trình hóa học
b) Tính nồng độ mol của dung dịch Ba(OH)2 đã dùng
c) Tính khối lượng chất kết tủa thu được.
Phương pháp giải
Với dạng bài tập CO2 tác dụng với Ba(OH)2, ta thực hiện các bước sau:
- Bước 1: Đổi số mol nCO2 = VCO2/22,4
- Bước 2: Viết phương trình hóa học, tính số mol các chất còn lại theo số mol CO2
- Bước 3: Tính nồng độ mol: CM = nBa(OH)2/VBa(OH)2 và tính khối lượng kết tủa theo số mol đã tính ở trên.
Hướng dẫn giải
Câu a: Phương trình hóa học
CO2 + Ba(OH)2 → BaCO3↓ + H2O
Câu b: Nồng độ mol của dung dịch Ba(OH)2 đã dùng
\({n_{C{O_2}}} = \frac{{2,24}}{{22,4}} = 0,1\;mol\)
Dựa vào phương trình trên ta thấy:
nBa(OH)2 = nCO2 = 0,1 mol
⇒ CM Ba(OH)2 = 0,1/0,2 = 0,5 mol/l
Câu c: Khối lượng chất kết tủa thu được
Dựa vào phương trình, ta có:
nBaCO3 = nCO2 = 0,1 mol
⇒ mBaCO3 = 0,1.197 = 19,7 (g).
B. Lưu huỳnh đioxit
1. Giải bài 1 trang 11 SGK Hóa lớp 9
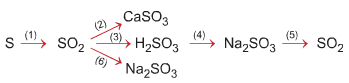
Viết phương trình hóa học cho mỗi chuyển đổi sau:
Phương pháp giải
Với dạng bài tập viết phương trình theo dãy chuyển hóa, cần nắm được tính chất hóa học của những chất có trong dãy. Dựa vào chất đầu và sản phẩm suy ra những chất còn thiếu.
Hướng dẫn giải
(1) S + O2 → SO2
(2) SO2 + CaO → CaSO3
Hay SO2 + Ca(OH)2 → CaSO3 + H2O
(3) SO2 + H2O → H2SO3
(4) H2SO3 + Na2O → Na2SO3 + H2O
(5) Na2SO3 + H2SO4 → Na2SO4 + SO2 ↑ + H2O
Không nên dùng phản ứng Na2SO3 + 2HCl → 2NaCl + SO2 + H2O vì HCl dễ bay hơi nên khí SO2 thu được sẽ không tinh khiết
(6) SO2 + 2NaOH → Na2SO3 + H2O
Hoặc SO2 + Na2O → Na2SO3
2. Giải bài 2 trang 11 SGK Hóa lớp 9
Hãy nhận biết từng chất trong mỗi nhóm chất sau bằng phương pháp hóa học
a) Hai chất rắn màu trắng là CaO và P2O5
b) Hai chất khí không màu là SO2 và O2
Viết các phương trình hóa học.
Phương pháp giải
Với bài tập nhận biết, cần nắm các nguyên tắc cơ bản sau:
- Đối với hỗn hợp rắn:
- Cần hòa vào nước để tạo dung dịch.
- Sau đó dựa vào tính chất hóa học đặc trưng và khác nhau của các chất có thể quan sát được, sử dụng phương pháp phù hợp để nhận biết.
- Đối với hỗn hợp khí: Dựa vào tính chất hóa học đặc trưng khác nhau có thể quan sát được của các khí, sục các khí vào các chất thích hợp để nhận biết.
Hướng dẫn giải
Câu a: Cho nước vào hai ống nghiệm có chứa CaO và P2O5. Sau đó cho quỳ tím vào mỗi dung dịch:
- Dung dịch nào làm đổi màu quỳ tím thành xanh là dung dịch bazơ, chất ban đầu là CaO.
- Dung dịch nào làm đổi màu quỳ tím thành đỏ là dung dịch axit, chất ban đầu là P2O5.
CaO + H2O → Ca(OH)2
P2O5 + 3H2O → 2H3PO4
Câu b: Có 2 cách nhận biết
- Cách 1:
- Lấy mẫu thử từng khí
- Lấy quỳ tím ẩm cho vào từng mẫu thử. Mẫu nào làm quỳ tím hóa đỏ là SO2, còn lại là O2
SO2 + H2O → H2SO3
- Cách 2:
- Dẫn lần lượt từng khí vào dung dịch nước vôi trong, nếu có kết tủa xuất hiện thì khí dẫn vào là SO2
SO2 + Ca(OH)2 → CaSO3 ↓ + H2O
- Nếu không có hiện tượng gì thì khí dẫn vào là khí O2. Để xác định là khí O2 ta dùng que đóm còn than hồng, que đóm sẽ bùng cháy trong khí oxi.
3. Giải bài 3 trang 11 SGK Hóa lớp 9
Có những khí ẩm (khí có lẫn hơi nước): cacbon đioxit, hiđro, oxi, lưu huỳnh đioxit. Khí nào có thể được làm khô bằng canxi oxit ? Giải thích.
Phương pháp giải
Với bài tập làm khô khí, cần nắm các nguyên tắc sau:
- Làm khô một chất là loại nước ra khỏi chất đó nhưng không làm chất đó biến thành chất khác.
- Những khí nào không tác dụng với CaO thì sẽ làm khô được khí đó.
Hướng dẫn giải
Làm khô một chất là loại nước ra khỏi chất đó nhưng không làm chất đó biến thành chất khác.
Như vậy CaO chỉ làm khô những chất không có phản ứng hóa học với CaO, đó là các chất H2, O2. Những chất không làm khô bằng CaO là CO2 và SO2, vì có phản ứng với CaO:
CaO + SO2 → CaSO3
CaO + CO2 → CaCO3
4. Giải bài 4 trang 11 SGK Hóa lớp 9
Có những chất khí sau: CO2, H2, O2, SO2, N2. Hãy cho biết chất nào có tính chất sau:
a) nặng hơn không khí.
b) nhẹ hơn không khí.
c) cháy được trong không khí.
d) tác dụng với nước tạo thành dung dịch axit.
e) làm đục nước vôi trong.
g) đổi màu giấy quỳ tím ẩm thành đỏ.
Phương pháp giải
a) Không khí có phân tử khối ≈ 29 (g/ mol) → những chất có phân tử khối lớn hơn 29 sẽ nặng hơn không khí
b) Những chất có phân tử khối nhỏ hơn 29 sẽ nhẹ hơn không khí
c) Các chất là có phản ứng với oxi sẽ cháy được trong không khí.
d) Các oxit axit sẽ tác dụng với nước tạo thành dung dịch axit.
e) Các oxit axit làm đục nước vôi trong.
d) Các oxit axit đổi màu giấy quỳ tím ẩm thành đỏ.
Hướng dẫn giải
Câu a: Những khí nặng hơn không khí: CO2, O2, SO2.
Vì Mkk = 29 g/mol.
MCO2 = 12 + 16.2 = 44 g/mol.
⇒ \({d_{C{O_2}/kk}} = \frac{{{M_{C{O_2}}}}}{{{M_{kk}}}} = \frac{{44}}{{29}} > 1\)⇒ CO2 nặng hơn không khí.
Tương tự: MO2 = 16.2 = 32 g/mol, MSO2 = 32 + 16.2 = 64 g/mol.
Câu b: Những khí nhẹ hơn không khí: H2, N2.
Mkk = 29 g/mol.
MH2 = 1.2 = 2 g/mol.
\( \to {d_{{H_2}/kk}} = \frac{{{M_{{H_2}}}}}{{{M_{kk}}}} = \frac{2}{{29}} < 1\)⇒ H2 nhẹ hơn không khí.
Tương tự: MN2 = 14.2 = 28 g/mol.
Câu c: Những khí cháy được trong không khí: H2
2H2 + O2 \(\xrightarrow{{{t^o}}}\) 2H2O
Câu d: Những khí tác dụng với nước tạo thành dung dịch axit: CO2, SO2
CO2 + H2O → H2CO3
SO2 + H2O → H2SO3
Câu e: Những khí làm đục nước vôi trong: CO2, SO2
Ca(OH)2 + CO2 → CaCO3 + H2O
Ca(OH)2 + SO2 → CaSO3 + H2O
Câu g: Những khí làm đổi màu quỳ tím ẩm thành đỏ: CO2, SO2
Quỳ tím ẩm → xảy ra phản ứng với nước tạo axit làm quỳ tím chuyển đỏ
CO2 + H2O → H2CO3
SO2 + H2O → H2SO3
5. Giải bài 5 trang 11 SGK Hóa lớp 9
Khí lưu huỳnh đioxit được tạo thành từ cặp chất nào sau đây ?
a) K2SO3 và H2SO4
b) K2SO4 và HCl
c) Na2SO3 và NaOH
d) Na2SO4 và CuCl2
e) Na2SO3 và NaCl
Viết phương trình hóa học.
Phương pháp giải
Để biết được khí lưu huỳnh đioxit được tạo thành từ cặp chất nào cần lưu ý:
- Axit H2SO3 không bền sẽ bị phân hủy thành SO2↑ + H2O.
- Điều kiện để 2 chất (muối + muối; muối + axit; muối + bazơ) tác dụng với nhau phải tạo ra chất kết tủa hoặc bay hơi.
Hướng dẫn giải
Trong các cặp chất trên, SO2 chỉ tạo ra từ cặp chất K2SO3 và H2SO4, vì có phản ứng sinh ra SO2:
K2SO3 + H2SO4 → K2SO4 + SO2 ↑ + H2O
6. Giải bài 6 trang 11 SGK Hóa lớp 9
Dẫn 112 ml khí SO2 (đktc) đi qua 700 ml dung dịch Ca(OH)2 có nồng độ 0,01 M, sản phẩm là muối canxi sunfit.
a) Viết phương trình hóa học
b) Tính khối lượng các chất sau phản ứng.
Phương pháp giải
Với dạng bài tập CO2 tác dụng với Ca(OH)2, ta thực hiện các bước sau:
- Bước 1: Đổi số mol của SO2 ; Ca(OH)2
- Bước 2: Viết phương trình hóa học, so sánh số mol Ca(OH)2 và SO2 để xác định chất nào hết, chất nào dư
- Bước 3: Xác định các chất sản phẩm theo mol chất phản ứng hết.
Hướng dẫn giải
Câu a: Phương trình hóa học của phản ứng
SO2 + Ca(OH)2 → CaSO3 + H2O
Câu b: Khối lượng các chất sau phản ứng
VSO2 = 112 ml = 0,112 lít; VCa(OH)2 = 700 ml = 0,7 lít
\({n_{S{O_2}}} = \frac{V}{{22,4}} = \frac{{0,112}}{{22,4}} = 0,005(mol)\)
nCa(OH)2 = CM.V = 0,01.0,7 = 0,007 (mol)
Lập tỉ lệ: \(\frac{{0,005}}{1} < \frac{{0,007}}{1}\)
→ SO2 hết Ca(OH)2 dư
Các chất sau phản ứng: Ca(OH)2 và CaSO3
nCa(OH)2 = nSO2 = 0,005 mol
⇒ nCa(OH)2 dư = 0,007 – 0,005 = 0,002 (mol)
mCa(OH)2 dư = n.M = 0,002 . 74 = 0,148 (g).
nCaSO3 = nSO2 = 0,005 mol → mCaSO3 = n.M = 0,005.120 = 0,6 (g).
Tham khảo thêm
- docx Giải bài tập SGK Hóa 9 Bài 1: Tính chất HH của oxit và Khái quát về sự PL oxit
- docx Giải bài tập SGK Hóa 9 Bài 3: Tính chất hóa học của axit
- docx Giải bài tập SGK Hóa 9 Bài 4: Một số axit quan trọng
- docx Giải bài tập SGK Hóa 9 Bài 5: Luyện tập TCHH của oxit và axit
- docx Giải bài tập SGK Hóa 9 Bài 7: Tính chất hóa học của bazơ
- docx Giải bài tập SGK Hóa 9 Bài 8: Một số bazơ quan trọng
- docx Giải bài tập SGK Hóa 9 Bài 9: Tính chất hóa học của muối
- docx Giải bài tập SGK Hóa 9 Bài 10: Một số muối quan trọng
- docx Giải bài tập SGK Hóa 9 Bài 11: Phân bón hóa học
- docx Giải bài tập SGK Hóa 9 Bài 12: Mối quan hệ giữa các loại hợp chất vô cơ
- docx Giải bài tập SGK Hóa 9 Bài 13: Luyện tập chương 1 Các loại hợp chất vô cơ
