Giải bài tập SGK Hóa 9 Bài 42: Luyện tập chương 4 Hiđrocacbon - Nhiên liệu
Giải bài tập 1, 2, 3, 4 trang 133 sách giáo khoa Hóa 9 được eLib sưu tầm và tổng hợp bên dưới đây. Tài liệu sẽ giúp các bạn học sinh hệ thống lại những kiến thức đã học trong bài, định hướng phương pháp giải các bài tập cụ thể. Ngoài ra việc tham khảo tài liệu còn giúp các bạn học sinh rèn luyện và nâng cao kỹ năng giải bài tập. Mời các bạn cùng tham khảo!
Mục lục nội dung

1. Giải bài 1 trang 133 SGK Hóa học 9
Viết công thức cấu tạo đầy đủ và thu gọn của các chất hữu cơ có công thức phân tử sau : C3H8 ; C3H6 ; C3H4.
Phương pháp giải
C3H8 : Chỉ chứa liên kết đơn
C3H6 : Chứa 1 liên kết đôi và mạch vòng
C3H4 : Chứa 1 liên kết ba, 2 liên kết đôi và mạch vòng
Hướng dẫn giải
Để viết công thức cấu tạo các chất ta nên xem xét chất đó thuộc loại nào, trong số các hiđrocacbon đã học để viết công thức cấu tạo cho phù hợp.
a. C3H8 có công thức giống CH4 (CnH2n+2) nên có công thức cấu tạo có 1 liên kết đơn: CH3-CH2-CH3
b. C3H6 công thức phân tử giống C2H4 (CnH2n) nên công thức cấu tạo có 1 liên kết đôi CH2=CH-CH3 và mạch vòng: 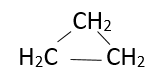
c. C3H4 công thức phân tử giống C2H2 (CnH2n-2) nên có công thức cấu tạo có 1 liên kết ba \(CH \equiv C - C{H_3}\); 2 nối đôi CH2=C=CH2 và mạch vòng: 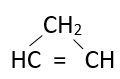
2. Giải bài 2 trang 133 SGK Hóa học 9
Có hai bình đựng hai chất khí là CH4, C2H4. Chỉ dùng dung dịch brom có thể phân biệt được hai chất khí trên không ? Nêu cách tiến hành.
Phương pháp giải
Sử dụng dung dịch brom: CH4 không làm mất màu dung dịch, C2H4 làm mất màu dung dịch
Hướng dẫn giải
Cho 2 khí vào bình có cùng thể tích, sau đó cho cùng một thể tích dung dịch brom có cùng nồng độ vào 2 bình và lắc đều lên. Quan sát hiện tượng.
+ Bình không làm thay đổi màu dung dịch brom là CH4.
+ Bình làm nhạt màu dung dịch brom là C2H4.
C2H4 + Br2 → C2H4Br2
3. Giải bài 3 trang 133 SGK Hóa học 9
Biết 0,01 mol hiđrocacbon X có thể tác dụng tối đa với 100 ml dung dịch brom 0,1 M. Vậy X là hiđrocacbon nào trong số các chất sau ?
A. CH4
B. C2H2
C. C2H4
D. C6H6
Phương pháp giải
Xét tỉ lệ nA : nBr2
→ Đáp án cần chọn
Hướng dẫn giải
nBr2 = 0,1 x 0,1 = 0,01 mol → Tỉ lệ mol giữa nA : nBr2 = 1: 1
Chứng tỏ trong A chứa một nối đôi C=C
Do đó A là C2H4
Phương trình hóa học: C2H4 + Br2 → C2H4Br2
4. Giải bài 4 trang 133 SGK Hóa học 9
Đốt cháy 3 gam chất hữu cơ A, thu được 8,8 gam khí CO2 và 5,4 gam H2O.
a) Trong chất hữu cơ A có những nguyên tố nào?
b) Biết phân tử khối của A nhỏ hơn 40. Tìm công thức phân tử của A.
c) Chất A có làm mất màu dung dịch brom không?
d) Viết phương trình hoá học của A với clo khi có ánh sáng.
Phương pháp giải
a) nCO2 → nC → mC
nH2O → nH → mH
So sánh mA với (mC + mH)
+ Nếu mA = mC + mH thì A chứa C, H
+ Nếu mA > mC + mH thì A chứa C, H, O.
Và mO = mA - mC - mH
b) Tính tỉ lệ các nguyên tố trong hợp chất đó → CTĐGN → CTPT (dựa vào dữ kiện liên quan đến khối lượng mol)
Hướng dẫn giải
a. \({n_{C{O_2}}} = \dfrac{{8,8}}{{44}} = 0,2\,\,mol\)
→ Bảo toàn nguyên tố C: \({n_C} = {n_{C{O_2}}} = 0,2\,\,mol \to {m_C} = 0,2.12 = 2,4g\)
\({n_{{H_2}O}} = \dfrac{{5,4}}{{18}} = 0,3\,\,mol\)
→ Bảo toàn nguyên tố H: \({n_H} = 2{n_{{H_2}O}} = 2.0,3 = 0,6\,\,mol \to {m_H} = 0,6.1 = 0,6g\)
Ta thấy: mC + mH = 2,4 + 0,6 = 3g = mA
→ Trong A chỉ chứa 2 nguyên tố C và H
b. Đặt công thức phân tử của A là CxHy
Ta có: x : y = nC : nH = 0,3 : 0,6 = 1:3
Vậy công thức phân tử của A có dạng (CH3)n
Mà MA < 40
→ (12 + 3.1).n < 40
+ Nếu n = 1 \( \to\) không hợp lý vì số nguyên tử H bị lẻ
+ Nếu n = 2 \( \to\) công thức phân tử của A là C2H6
c. Trong phân tử A chỉ có liên kết đơn nên A không làm mất màu dung dịch brom
d. PTHH: \({C_2}{H_6} + C{l_2}\xrightarrow{{a/s}}{C_2}{H_5}Cl + HCl\)
Tham khảo thêm
- doc Giải bài tập SGK Hóa 9 Bài 34: Khái niệm về hợp chất hữu cơ và hóa học hữu cơ
- doc Giải bài tập SGK Hóa 9 Bài 35: Cấu tạo phân tử hợp chất hữu cơ
- doc Giải bài tập SGK Hóa 9 Bài 36: Metan
- doc Giải bài tập SGK Hóa 9 Bài 37: Etilen
- doc Giải bài tập SGK Hóa 9 Bài 38: Axetilen
- doc Giải bài tập SGK Hóa 9 Bài 39: Benzen
- doc Giải bài tập SGK Hóa 9 Bài 40: Dầu mỏ và khí thiên nhiên
- doc Giải bài tập SGK Hóa 9 Bài 41: Nhiên liệu
