Giải bài tập SGK Hóa 10 Bài 13: Liên kết cộng hóa trị
Bài này sẽ giúp các em nắm vững được lý thuyết cũng như cách giải các bài tập của bài Liên kết cộng hóa trị với cách làm đầy đủ, chi tiết và rõ ràng. Hy vọng đây sẽ là tài liệu tham khảo hữu ích cho các em học sinh
Mục lục nội dung

1. Giải bài 1 trang 64 SGK Hóa học 10
Chọn câu đúng nhất về liên kết cộng hóa trị.
Liên kết cộng hóa trị là liên kết
A. Giữa các phi kim với nhau.
B. Trong đó cặp electron chung bị lệch về một nguyên tử.
C. Được hình thành do sự dùng chung electron của 2 nguyên tử khác nhau.
D. Được tạo nên giữa 2 nguyên tử bằng một hay nhiều cặp electron chung.
Phương pháp giải
Xem lại lý thuyết về liên kết cộng hóa trị
Hướng dẫn giải
Liên kết cộng hóa trị là liên kết được tạo nên giữa 2 nguyên tử bằng một hay nhiều cặp electron chung.
⇒ Đáp án đúng là D.
2. Giải bài 2 trang 64 SGK Hóa học 10
Chọn câu đúng trong các câu sau:
A. Trong liên kết cộng hóa trị, cặp electron lệch về phía nguyên tử có độ âm điện nhỏ hơn.
B. Liên kết cộng hóa trị có cực được tạo thành giữa 2 nguyên tử có hiệu độ âm điện từ 0,4 đến nhỏ hơn 1,7.
C. Liên kết cộng hóa trị không có cực được tạo nên từ các nguyên tử khác hẳn nhau về tính chất hóa học.
D. Hiệu độ âm điện giữa 2 nguyên tử lớn thì phân tử phân cực yếu.
Phương pháp giải
Xem lại lý thuyết về liên kết cộng hóa trị → phân tích từng nhận định
→ Lựa chọn đúng, sai
Hướng dẫn giải
A. sai vì cặp liên kết CHT phải lệch về phía nguyên tử có độ âm điện lớn hơn.
B. đúng
C. sai vì liên kết CHT không phân cực được tạo nên từ các nguyên tử có tính chất hóa học tương tự gần giống nhau
D. sai hiệu độ âm điện của 2 nguyên tử càng lớn thì phân tử càng phân cực mạnh
Đáp án B
3. Giải bài 3 trang 64 SGK Hóa học 10
Độ âm điện của một nguyên tử đặc trưng cho:
A. Khả năng hút electron của nguyên tử đó khi hình thành liên kết hóa học.
B. Khả năng nhường electron của nguyên tử đó cho nguyên tử khác.
C. Khả năng tham gia phản ứng mạnh hay yếu của nguyên tử đó.
D. Khả năng nhường proton của nguyên tử đó cho nguyên tử khác.
Phương pháp giải
Xem lại lý thuyết về liên kết cộng hóa trị, tả lời câu hỏi độ âm điện đặc trưng cho giá trị nào?
Hướng dẫn giải
Độ âm điện của một nguyên tử đặc trưng cho khả năng hút electron của nguyên tử đó khi hình thành liên kết hóa học.
⇒ Đáp án đúng là A.
4. Giải bài 4 trang 64 SGK Hóa học 10
Thế nào là liên kết ion, liên kết cộng hóa trị không cực, liên kết cộng hóa trị có cực? Cho thí dụ minh họa.
Phương pháp giải
- Xem lại lý thuyết về liên kết cộng hóa trị, liên kết ion
- Lấy ví dụ minh họa
Hướng dẫn giải
- Liên kết ion là liên kết được hình thành bởi lực hút tĩnh điện giữa các ion mang điện tích trái dấu.
Thí dụ: K+ + Cl- → KCl
Liên kết cộng hóa trị không cực là liên kết được tạo nên giữa hai nguyên tử bằng những cặp electron chung.
Thí dụ:
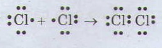
Liên kết cộng hóa trị trong đó những cặp electron chung bị lệch về phía một nguyên tử được gọi là liên kết cộng hóa trị có cực.
Thí dụ:
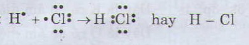
5. Giải bài 5 trang 64 SGK Hóa học 10
Dựa vào hiệu độ âm điện các nguyên tố, hãy cho biết có loại liên kết nào trong các chất sau đây :
AlCl3, CaCl2, CaS, Al2S3?
Lấy giá trị độ âm điện của các nguyên tố ở bảng 6 trang 45
Phương pháp giải
Lấy độ âm điện của nguyên tử có độ âm điện lớn trừ đi độ âm điện của nguyên tử có độ âm điện nhỏ hơn nếu:
+ Hiệu độ âm điện < 0,4 → liên kết CHT không cực
+ Hiệu độ âm điện từ 0,4 đến < 1,7 → liên kết CHT có cực
+ Hiệu độ âm điện ≥ 1,7 → liên kết ion
Hướng dẫn giải
Hiệu độ âm điện:
AlCl3 là: 3,16 – 1,61 = 1,55 → liên kết CHT phân cực
CaCl2: 3,16 – 1,00 = 2,16 → liên kết ion
CaS : 2,58 – 1,00 = 1,58 → liên kết CHT có cực
Al2S3: 2,58 – 1,61 = 0,97 → liên kết CHT có cực
6. Giải bài 6 trang 64 SGK Hóa học 10
Viết công thức electron và công thức cấu tạo các phân tử sau: Cl2, CH4, C2H4, C2H2, NH3.
Phương pháp giải
Dựa vào cấu hình electron và lý thuyết liên kết cộng hóa trị giữa các nguyên tố hóa học để viết công thức e và công thức cấu tạo
Hướng dẫn giải
Cl2:
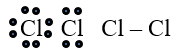
CH4:
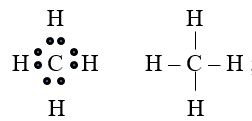
C2H4:
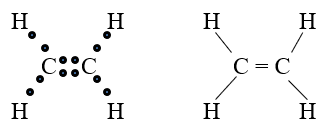
C2H2:
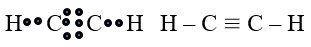
NH3:
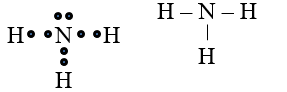
7. Giải bài 7 trang 64 SGK Hóa học 10
X, A, Z là những nguyên tố có số điện tích hạt nhân là 9, 19, 8.
a) Viết cấu hình electron nguyên tử của các nguyên tố đó.
b) Dự đoán liên kết hóa học có thể có giữa các cặp X và A, A và Z, Z và X.
Phương pháp giải
a) Cách viết cấu hình electron
Bước 1: Dãy phân bố thứ tự mức năng lượng
1s 2s 2p 3s 3p 4s 3d 4p 5s
Bước 2: Điền các electron vào các phân lớp
s: 2e ; p : 6e ; d : 10e; f: 14e
Bước 3: Hoàn chỉnh cấu hình electron
b) phi kim mạnh với kim loại mạnh => liên kết ion
Hướng dẫn giải
a) 9X : 1s2 2s2 2p5
Đây là F có độ âm điện là 3,98.
19A : 1s2 2s2 2p6 3s2 3p6 4s1
Đây là K có độ âm điện là 0,82.
8Z: 1s2 2s2 2p4
Đây là O có độ âm điện là 3,44.
b) Cặp X và A, hiệu số độ âm điện là: 3,98 – 0,82 = 3,16 , có liên kết ion.
Cặp A và Z, hiệu số độ âm điện là: 3,44 – 0,82 = 2,62, có liên kết ion.
Cặp X và Z, hiệu số độ âm điện là: 3,98 – 3,44 = 0,54, có liên kết cộng hóa trị có cực.
