Giải bài tập SGK Hóa 8 Bài 20: Tỉ khối của chất khí
Hướng dẫn Giải bài tập Hóa học 8 Bài 20 dưới đây sẽ giúp các em học sinh nắm vững phương pháp giải bài tập và ôn luyện tốt kiến thức về tỉ khối của chất khí. Mời các em cùng theo dõi.
Mục lục nội dung

1. Giải bài 1 trang 69 SGK Hóa học 8
Có những khí sau: N2, O2,Cl2, CO, SO2.
Hãy cho biết:
a) Những khí nào nặng hay nhẹ hơn khí hiđro bao nhiêu lần?
b) Những khí nào nặng hơn hay nhẹ hơn không khí bao nhiêu lần?
Phương pháp giải
Công thức tính tỉ khối của:
- Khí A đối với khí B: dA/B = MA / MB
- Khí A đối với không khí: dA/kk = MA/29
Hướng dẫn giải
Câu a
Trong số các chất khí, khí hiđro nhẹ nhất. Tỉ khối của các khí đối với hiđro:
- dN2/H2 = 28 / 2 = 14 lần ⇒ Vậy khí N2 nặng hơn khí H2 14 lần.
- dO2/H2 = 32 / 2 = 16 lần ⇒ Vậy khí O2 nặng hơn khí H2 16 lần.
- dCl2/H2 = 71 / 2 = 35,5 lần ⇒ Vậy khí Cl2 nặng hơn khí H2 35,5 lần.
- dCO/H2 = 28 / 2 = 14 lần ⇒ Vậy khí CO nặng hơn khí H2 14 lần.
- dSO2/H2 = 64 / 2 = 32 lần ⇒ Vậy khí SO2 nặng hơn khí H2 32 lần.
Câu b
Tỉ khối của các khí đối với không khí:
- dN2/kk = 28 / 29 ≈ 0,965 ⇒ N2 nhẹ hơn không khí 0,965 lần.
- dO2/kk = 32 / 29 ≈ 1,10 ⇒ O2 nặng hơn không khí 1,10 lần.
- dCl2/kk = 71 / 29 ≈ 2,448 ⇒ Cl2 nặng hơn không khí 2,448 lần.
- dCO/kk = 28 / 29 ≈ 0,965 ⇒ CO nhẹ hơn không khí 0,965 lần.
- dSO2/kk = 64 / 29 ≈ 2,21 ⇒ SO2 nặng hơn không khí 2,21 lần.
2. Giải bài 2 trang 69 SGK Hóa học 8
Hãy tìm khối lượng mol của những khí:
a) Có tỉ khối đối với oxi là: 1,375; 0,0625.
b) Có tỉ khối đối với không khí là: 2,207; 1,172.
Phương pháp giải
Công thức tính tỉ khối của:
- Khí A đối với khí B: dA/B = MA / MB
- Khí A đối với không khí: dA/kk = MA/29
Hướng dẫn giải
Câu a
\({d_{X/{O_2}}} = \frac{{{M_X}}}{{32}} \Rightarrow {M_X} = 32.{d_{X/{O_2}}}\)
Khối lượng mol của các khí lần lượt là:
- M1 = 1,375 . 32 = 44 g/mol.
- M2 = 0,0625 . 32 = 2 g/mol.
Câu b
\({d_{X/KK}} = \frac{{{M_X}}}{{29}} \Rightarrow {M_X} = 29.{d_{X/kk}}\)
Khối lượng mol của các khí lần lượt là:
- M1 = 29 . 2,207 = 64 g/mol.
- M2 = 29 . 1,172 = 34 g/mol.
3. Giải bài 3 trang 69 SGK Hóa học 8
Có thể thu những khí nào vào bình (từ những thí nghiệm trong phòng thí nghiệm): khí hiđro; khí clo; khí cacbon đioxit, khí metan CH4 bằng cách:
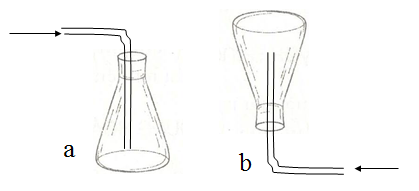
a) Đặt đứng bình?
b) Đặt ngược bình?
Phương pháp giải
- Những khí nặng hơn không khí có thể thu được bằng cách đặt đứng bình.
- Những khí nhẹ hơn không khí có thể thu được bằng cách đặt ngược bình.
Hướng dẫn giải
Ta có:
\({d_{{H_2}/kk}} = \frac{{{M_{{H_2}}}}}{{{M_{kk}}}} = \frac{2}{{29}} = 0,07\)
\({d_{{Cl_2}/kk}} = \frac{{{M_{{Cl_2}}}}}{{{M_{kk}}}} = \frac{71}{{29}} = 2,45\)
\({d_{{CO_2}/kk}} = \frac{{{M_{{CO_2}}}}}{{{M_{kk}}}} = \frac{44}{{29}} = 1,52\)
\({d_{{CH_4}/kk}} = \frac{{{M_{{CH_4}}}}}{{{M_{kk}}}} = \frac{16}{{29}} = 0,55\)
Câu a
Khi đặt đứng bình ta sẽ thu được những chất khí nặng hơn không khí (có tỉ khối đối với không khí lớn hơn 1) như khí clo (nặng hơn 2,45 lần), khí cacbon đioxit (1,52 lần).
Câu b
Khi đặt ngược bình ta sẽ thu được những chất nhẹ hơn không khí (có tỉ khối đối với không khí nhỏ hơn 1) như khí hiđro (nhẹ hơn 0,07 lần), khí metan (nhẹ hơn 0,55 lần).
Tham khảo thêm
- doc Giải bài tập SGK Hóa 8 Bài 18: Mol
- doc Giải bài tập SGK Hóa 8 Bài 19: Chuyển đổi giữa khối lượng, thể tích và lượng chất
- doc Giải bài tập SGK Hóa 8 Bài 21: Tính theo công thức hóa học
- doc Giải bài tập SGK Hóa 8 Bài 22: Tính theo phương trình hóa học
- doc Giải bài tập SGK Hóa 8 Bài 23: Bài luyện tập 4