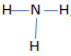Giải bài tập SBT Hóa 8 Bài 10: Hóa trị
Hướng dẫn Giải bài tập Sách bài tập Hóa học 8 Bài 10 dưới đây sẽ giúp các em học sinh nắm vững phương pháp giải bài tập và ôn luyện tốt kiến thức về hóa trị. Mời các em cùng theo dõi.
Mục lục nội dung
1. Giải bài 10.1 trang 14 SBT Hóa học 8
2. Giải bài 10.2 trang 14 SBT Hóa học 8
3. Giải bài 10.3 trang 14 SBT Hóa học 8
4. Giải bài 10.4 trang 14 SBT Hóa học 8
5. Giải bài 10.5 trang 14 SBT Hóa học 8
6. Giải bài 10.6 trang 14 SBT Hóa học 8
7. Giải bài 10.7 trang 14 SBT Hóa học 8
8. Giải bài 10.8 trang 15 SBT Hóa học 8

1. Giải bài 10.1 trang 14 SBT Hóa học 8
Chép vào vở bài tập những câu sau đây với đầy đủ các từ hay cụm từ thích hợp chọn trong khung.
Hóa trị, nguyên tử, nguyên tố, nhóm nguyên tử, khả năng liên kết, phân tử.
"Hóa trị là con số biểu thị ... của ... nguyên tố này (hay ...) với ... nguyên tố khác. Hóa trị của một ... (hay ...) được xác định theo ... của H chọn là đơn vị và ... của O là hai đơn vị".
Phương pháp giải
Để trả lời các câu hỏi trên cần nắm rõ lý thuyết về hóa trị.
Hướng dẫn giải
"Hoá trị là con số biểu thị khả năng liên kết của nguyên tử nguyên tố này (hay nhóm nguyên tử) với nguyên tử nguyên tố khác. Hoá trị của một nguyên tố (hay nhóm nguyên tử) được xác định theo hoá trị của H chọn làm đơn vị và hoá trị của O là hai đơn vị."
2. Giải bài 10.2 trang 14 SBT Hóa học 8
Người ta quy ước mỗi vạch ngang giữa kí hiệu biểu thị một hóa trị của mỗi bên nguyên tử. Cho biết sơ đồ công thức của hợp chất giữa nguyên tố X, Y với H và O như sau: H - X - H; X = O; H - Y
a) Tính hóa trị của X và Y.
b) Viết sơ đồ công thức hợp chất giữa nguyên tố Y và O, giữa nguyên tố X và Y.
Phương pháp giải
Để trả lời các câu hỏi trên cần nắm rõ lý thuyết về hóa trị. Đồng thời dựa vào hóa trị của H và O để suy ra hóa trị của các nguyên tố còn lại và công thức hợp chất giữa nguyên tố Y và O, giữa nguyên tố X và Y.
Hướng dẫn giải
a) X hoá trị II, Y hoá trị I
b) Y - O - Y, Y - X - Y.
3. Giải bài 10.3 trang 14 SBT Hóa học 8
Viết sơ đồ công thức của các hợp chất sau: HCl, H2O, NH3,CH4.
Phương pháp giải
Để viết sơ đồ công thức của các hợp chất trên cần nắm rõ lý thuyết về hóa trị.
Hướng dẫn giải
a) HCl: H-Cl
b) H2O: H-O-H
c) NH3:
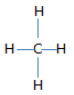
d) CH4:
4. Giải bài 10.4 trang 14 SBT Hóa học 8
Tính hóa trị của mỗi nguyên tố trong công thức phân tử các hợp chất sau. Cho biết S hóa trị II:
K2S, MgS, Cr2S3, CS2
Phương pháp giải
Cần nắm rõ lý thuyết về cách tính hóa trị:
Quy tắc hóa trị x. a = y. b
Biết x, y và a (hoặc b) thì tính được b (hoặc a)
Biết a , b thì tìm được x, y để lập công thức hóa học. chuyển thành tỉ lệ: x/y=b/a=b′/a′
Lấy x = b hay b’ và y = a’ (nếu a’, b’ là những số đơn giản hơn so với a, b).
Hướng dẫn giải
a) K2S: Gọi a là hóa trị của K.
Theo quy tắc hóa trị: a.2 = II.1 → a = (II.1) : 2 = I
Vậy K có hóa trị I.
b) MgS: Gọi b là hóa trị của Mg.
Theo quy tắc hóa trị: b.1 = II.1 → b = (II.1) : I = II
Vậy Mg có hóa trị II.
c) Cr2S3: Gọi c là hóa trị của Cr.
Theo quy tắc hóa trị: c.2 = II.3 → c = (II.3) : 2 = III.
Vậy Cr có hóa trị III.
d) CS2:
Theo quy tắc hóa trị: d.1 = II.2 → d = (II.2) : 1 = IV.
Vậy C có hóa trị IV.
5. Giải bài 10.5 trang 14 SBT Hóa học 8
Tính hóa trị của mỗi nguyên tố trong công thức phân tử các hợp chất sau, biết nhóm (NO3) hóa trị I và nhóm (CO3) hóa trị II: Ba(NO3)2; Fe(NO3)3; CuCO3; Li2CO3.
Phương pháp giải
Cần nắm rõ lý thuyết về cách tính hóa trị:
Quy tắc hóa trị x. a = y. b
Biết x, y và a (hoặc b) thì tính được b (hoặc a)
Biết a , b thì tìm được x, y để lập công thức hóa học. chuyển thành tỉ lệ: x/y=b/a=b′/a′
Lấy x = b hay b’ và y = a’ (nếu a’, b’ là những số đơn giản hơn so với a, b).
Hướng dẫn giải
a) Ba(NO3)2: Gọi hóa trị của Ba là a.
Theo quy tắc hóa trị: a.1 = I.2 → a = (I.2) : 1 = II.
Vậy Ba có hóa trị II.
b) Fe(NO3)3: Gọi hóa trị của Fe là b.
Theo quy tắc hóa trị: b.1 = I.3 → b = (I.3) : 1 = III.
Vậy Fe có hóa trị III.
c) CuCO3: Gọi hóa trị của Cu là c.
Theo quy tắc hóa trị: c.1 = II.1 → c = (II.1) : 1 = II>
Vậy Cu có hóa trị II.
d) Li2CO3: Gọi hóa trị của Li là d.
Theo quy tắc hóa trị: d.2 = II.1 → d = (II.1) : 2 = I.
Vậy Li có hóa trị I.
6. Giải bài 10.6 trang 14 SBT Hóa học 8
Lập công thức hóa học của những chất hai nguyên tố như sau:
Si(IV) và H
P(V) và O;
Fe(III) và Br(I)
Ca và N(III)
Phương pháp giải
Để lập công thức hóa học của những chất hai nguyên tố, ta cần nắm rõ quy tắc hóa trị:
Quy tắc hóa trị x. a = y. b
Biết x, y và a (hoặc b) thì tính được b (hoặc a)
Biết a , b thì tìm được x, y để lập công thức hóa học. chuyển thành tỉ lệ: x/y=b/a=b′/a′
Lấy x = b hay b’ và y = a’ (nếu a’, b’ là những số đơn giản hơn so với a, b).
Hướng dẫn giải
a) Si (IV) và H:
Theo quy tắc hóa trị: IV.x = y.I
Tỉ lệ: \(\frac{x}{y} = \frac{I}{{IV}} \to \left\{ \begin{array}{l}
x = 1\\
y = 4
\end{array} \right.\)
Vậy công thức hóa học của SixHy là SiH4.
b) P(V) và O:
Theo quy tắc hóa trị: V.x = II.y
Tỉ lệ: \(\frac{x}{y} = \frac{{II}}{V} \to \left\{ \begin{array}{l}
x = 2\\
y = 5
\end{array} \right.\)
Vậy công thức hóa học của PxOy là P2O5.
c) Fe(III) và Br(I):
Theo quy tắc hóa trị: III.x = I.y
Tỉ lệ: \(\frac{x}{y} = \frac{I}{{III}} \to \left\{ \begin{array}{l}
x = 1\\
y = 3
\end{array} \right.\)
Vậy công thức hóa học của FexBry là FeBr3.
d) Ca và N(III):
Theo quy tắc hóa trị: II.x = III.y
Tỉ lệ: \(\frac{x}{y} = \frac{{III}}{{II}} \to \left\{ \begin{array}{l}
x = 3\\
y = 2
\end{array} \right.\)
Vậy công thức hóa học của CaxNy là Ca3N2.
7. Giải bài 10.7 trang 14 SBT Hóa học 8
Lập công thức hóa học của những chất hợp chất tạo bởi một nguyên tố và nhóm nguyên tử như sau:
a) Ba và nhóm (OH)
b) Al và nhóm (NO3)
c) Cu(II) và nhóm (CO3)
d) Na và nhóm (PO4)(III)
Phương pháp giải
Để lập công thức hóa học của những chất hợp chất tạo bởi một nguyên tố và nhóm nguyên tử, ta cần nắm rõ quy tắc hóa trị:
Quy tắc hóa trị x. a = y. b
Biết x, y và a (hoặc b) thì tính được b (hoặc a)
Biết a , b thì tìm được x, y để lập công thức hóa học. chuyển thành tỉ lệ: x/y=b/a=b′/a′
Lấy x = b hay b’ và y = a’ (nếu a’, b’ là những số đơn giản hơn so với a, b).
Hướng dẫn giải
a) Ba và nhóm (OH): Bax(OH)y
Theo quy tắc hóa trị: II.x = I.y
Tỉ lệ: \(\frac{x}{y} = \frac{I}{{II}} \to \left\{ \begin{array}{l}
x = 1\\
y = 2
\end{array} \right.\)
Vậy công thức hóa học của Bax(OH)y là Ba(OH)2.
b) Al và nhóm (NO3): Alx(NO3)y
Theo quy tắc hóa trị: III.x = I.y
Tỉ lệ: \(\frac{x}{y} = \frac{I}{{III}} \to \left\{ \begin{array}{l}
x = 1\\
y = 3
\end{array} \right.\)
Vậy công thức hóa học của Alx(NO3)y là Al(NO3)3.
c) Cu(II) và nhóm (CO3): Cux(CO3)y
Theo quy tắc hóa trị: II.x = II.y
Tỉ lệ: \(\frac{x}{y} = \frac{{II}}{{II}} \to \left\{ \begin{array}{l}
x = 1\\
y = 1
\end{array} \right.\)
Vậy công thức hóa học của Cux(CO3)y là CuCO3.
d) Na và nhóm (PO4)(III): Nax(PO4)y
Theo quy tắc hóa trị: I.x = III.y
Tỉ lệ: \(\frac{x}{y} = \frac{{III}}{I} \to \left\{ \begin{array}{l}
x = 3\\
y = 1
\end{array} \right.\)
Vậy công thức hóa học của Nax(PO4)y là Na3PO4.
8. Giải bài 10.8 trang 15 SBT Hóa học 8
Biết Cr (crom) có 2 hóa trị thường gặp là II và III, hãy chọn công chức hóa học đúng trong số các công thức cho sau đây:
(1) CrSO4 ; (2) Cr2SO4 ; (3) CrO; (4) CrO2
(5) Cr(SO4)2 ; (6) Cr2(SO4)3; (7) Cr2O; (8) Cr2O3
b) Tính phân tử khối của những chất biểu diễn bởi công thức hoá học đúng.
Phương pháp giải
a) Xem lại lý thuyết về hóa trị:
Quy tắc hóa trị x. a = y. b
Biết x, y và a (hoặc b) thì tính được b (hoặc a)
Biết a , b thì tìm được x, y để lập công thức hóa học. chuyển thành tỉ lệ: x/y=b/a=b′/a′
Lấy x = b hay b’ và y = a’ (nếu a’, b’ là những số đơn giản hơn so với a, b).
b) Xem lại cách tính phân tử khối:
Công thức hóa học: Dùng để biểu diễn chất gồm một kí hiệu hóa học (đơn chất) hay hai, ba.. kí hiệu hóa học (hợp chất) và chỉ số ghi ở mỗi chân kí hiệu.
Hướng dẫn giải
a) Những công thức hoá học đúng:
Cr hoá trị II : CrSO4, CrO.
Cr hoá trị III : Cr2(SO4)3, Cr2O3.
b) Phân tử khối của những chất biểu diễn bởi các công thức hoá học này :
CrSO4 = 52 + 32 + 4.16 = 148 (đvC)
CrO = 52 + 16 = 68 (đvC).
Cr2(SO4)3 = 2.52 + 3(32 + 4.16) = 392 (đvC)
Cr2O3 = 2.52 + 3.16 = 152 (đvC).
9. Giải bài 10.9 trang 15 SBT Hóa học 8
Người ta xác định được rằng nguyên tố silic(Si) chiếm 87,5% về khối lượng trong hợp chất với nguyên tố hidro.
a) Viết công thức hóa học và tính phân tử khối của hợp chất.
b) Xác định hóa trị của Silic trong hợp chất.
Phương pháp giải
a) Gọi công thức của hợp chất là SixHy.
Theo đề bài ta có:
\(\frac{{28x}}{y} = \frac{{87,5\% }}{{(100 - 87,5)}} \to \frac{x}{y} = \frac{1}{4} \to \left\{ \begin{array}{l}
x = ?\\
y = ?
\end{array} \right.\)
b) Từ công thức vừa tìm, suy ra hóa trị của Si.
Hướng dẫn giải
a) Gọi công thức của hợp chất là SixHy.
Theo đề bài ta có:
\(\frac{{28x}}{y} = \frac{{87,5\% }}{{(100 - 87,5)}} \to \frac{x}{y} = \frac{1}{4} \to \left\{ \begin{array}{l}
x = 1\\
y = 4
\end{array} \right.\)
CTHH của hợp chất là SiH4.
Phân tử khối là: 28 + 4.1 = 32 ( đvC)
b) Hóa trị của Si trong hợp chất SiH4 là IV.
10. Giải bài 10.10 trang 15 SBT Hóa học 8
Phân tích một mẫu hợp chất tạo bởi hai nguyên tố là sắt và oxi. Kết quả cho thấy cứ 7 phần khối lượng sắt có tương ứng với 3 phần khối lượng oxi.
a) Viết công thức hóa học và tính phân tử khối của hợp chất.
b) Xác định hóa trị của sắt trong hợp chất.
Phương pháp giải
a) Công thức chung của hợp chất FexOy
Theo đề bài ta có:
\(\frac{{m_Fe}}{m_O} = \frac{{7 }}{{(3)}} \to \frac{56x}{16y} = \frac{7}{3} \to \left\{ \begin{array}{l}
x = ?\\
y = ?
\end{array} \right.\)
Suy ra công thức hóa học.
b) Từ công thức vừa tìm được suy ra hóa trị của Fe.
Hướng dẫn giải
a) Công thức chung của hợp chất FexOy.
Theo đề bài ta có:
\(\frac{{m_Fe}}{m_O} = \frac{{7 }}{{(3)}} \to \frac{56x}{16y} = \frac{7}{3} \to \left\{ \begin{array}{l}
x = 2\\
y = 3
\end{array} \right.\)
Vậy CTHH của hợp chất là Fe2O3.
Phân tử khối là: 56.2 + 16.3 = 160 (đvC)
b) Hợp chất Fe2O3
Gọi hóa trị của Fe là x
Theo quy tắc hóa trị ta có: x. 2 = 3.II ⇒ x = III
Vậy hóa trị của sắt là III.
Tham khảo thêm
- doc Giải bài tập SBT Hóa 8 Bài 2: Chất
- doc Giải bài tập SBT Hóa 8 Bài 4: Nguyên tử
- doc Giải bài tập SBT Hóa 8 Bài 5: Nguyên tố hóa học
- doc Giải bài tập SBT Hóa 8 Bài 6: Đơn chất- Hợp chất- Phân tử
- doc Giải bài tập SBT Hóa 8 Bài 8: Luyện tập
- doc Giải bài tập SBT Hóa 8 Bài 9: Công thức hóa học
- doc Giải bài tập SBT Hóa 8 Bài 11: Luyện tập chương 1