Giải bài tập SBT Hóa 8 Bài 24: Tính chất của oxi
Hướng dẫn Giải bài tập Sách bài tập Hóa học 8 Bài 24 dưới đây sẽ giúp các em học sinh nắm vững phương pháp giải bài tập và ôn luyện tốt kiến thức về tính chất của oxi. Mời các em cùng theo dõi.
Mục lục nội dung
1. Giải bài 24.1 trang 32 SBT Hóa học 8
2. Giải bài 24.2 trang 32 SBT Hóa học 8
3. Giải bài 24.3 trang 32 SBT Hóa học 8
4. Giải bài 24.4 trang 32 SBT Hóa học 8
5. Giải bài 24.5 trang 33 SBT Hóa học 8
6. Giải bài 24.6 trang 33 SBT Hóa học 8
7. Giải bài 24.7 trang 33 SBT Hóa học 8
8. Giải bài 24.8 trang 33 SBT Hóa học 8
9. Giải bài 24.9 trang 33 SBT Hóa học 8
10. Giải bài 24.10 trang 33 SBT Hóa học 8
11. Giải bài 24.11 trang 34 SBT Hóa học 8
12. Giải bài 24.12 trang 34 SBT Hóa học 8
13. Giải bài 24.13 trang 34 SBT Hóa học 8
14. Giải bài 24.14 trang 34 SBT Hóa học 8
15. Giải bài 24.15 trang 34 SBT Hóa học 8
16. Giải bài 24.16 trang 34 SBT Hóa học 8
17. Giải bài 24.17 trang 34 SBT Hóa học 8

1. Giải bài 24.1 trang 32 SBT Hóa học 8
Phát biểu nào sau đây đúng ?
A. Oxi là chất khí tan ít trong nước và nhẹ hơn không khí.
B. Oxi là chất khí tan vô hạn trong nước và nặng hơn không khí.
C. Khí oxi dễ dàng tác dụng được với nhiều đơn chất (kim loại, phi kim) và hợp chất.
D. Ở nhiệt độ cao, khí oxi dễ dàng tác dụng được với nhiều đơn chất (kim loại, phi kim) và hợp chất.
Phương pháp giải
Dựa vào tính chất vật lí và hóa học của oxi để lựa chọn đáp án đúng. Đồng thời, với ý đúng nên viết phương trình hóa học để minh h
Hướng dẫn giải
3Fe + 2O2 → Fe3O4
S + O2 → SO2
CH4 + 2O2 → CO2 + 2H2O
⇒ Chọn D.
2. Giải bài 24.2 trang 32 SBT Hóa học 8
Viết phương trình hóa học của phản ứng giữa O2 với:
a) 3 kim loại hóa trị I, II, III.
b) 3 phi kim, thí dụ như C, S, P,…
c) 3 hợp chất, thí dụ như:
• Khí ga (butan C4H10) sinh ra khí cacbonic và nước.
• Khí ammoniac (NH3) sinh ra khí nito và nước.
• Khí hidro sunfua (H2S) sinh ra khí sunfuaro và nước.
Phương pháp giải
Dựa vào tính chất hóa học của oxi, đồng thời ghi nhớ công thức hóa học của oxi ghi kết hợp với kim loại và phi kim để viết phương trình hóa học đúng.
Hướng dẫn giải
Phương trình hóa học của phản ứng giữa O2 với:
a) 3 kim loại:
4Na + O2 \(\xrightarrow{{{t^o}}}\) 2Na2O
2Mg + O2 \(\xrightarrow{{{t^o}}}\) 2MgO
4Al + 3O2 \(\xrightarrow{{{t^o}}}\) 2Al2O3
b) 3 phi kim:
C + O2 \(\xrightarrow{{{t^o}}}\) CO2
S + O2 \(\xrightarrow{{{t^o}}}\) SO2
4P + 5O2 \(\xrightarrow{{{t^o}}}\) 2P2O5
c) 3 hợp chất:
C4H10 + 13O2 \(\xrightarrow{{{t^o}}}\) 8CO2 + 10H2O
4NH3 + 3O2 \(\xrightarrow{{{t^o}}}\) 2N2 + 6H2O
2H2S + 3O2 \(\xrightarrow{{{t^o}}}\) 2SO2 + 2H2O
3. Giải bài 24.3 trang 32 SBT Hóa học 8
Oxi trong không khí là đơn chất hay hợp chất? Vì sao cá sống được trong nước? Những lĩnh vực hoạt nào của con người cần thiết phải dùng bình nén oxi để hô hấp?
Phương pháp giải
Để trả lời những câu hỏi trên cần ghi nhớ: Oxi trong không khí là đơn chất. Trong nước có oxi hòa tan. Trong môi trường không có oxi cần dùng đến bình nén oxi để hô hấp.
Hướng dẫn giải
Oxi trong không khí là đơn chất.
Cá sống được trong nước vì trong nước có hoà tan khí oxi.
Những lĩnh vực hoạt động của con người cần thiết phải dùng bình nén oxi để hô hấp là : thợ lặn, phi công lái máy bay, phi công vũ trụ, bệnh nhân khó thở, công nhân làm việc ở các hầm mỏ sâu...
4. Giải bài 24.4 trang 32 SBT Hóa học 8
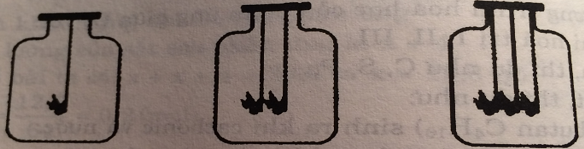
Trong 3 bình giống hệt nhau và có chứa thể tích oxi như nhau. Đồng thời ta cho vào 3 bình: bình 1 một cục than đang cháy, bình 2 hai cục than đang cháy, bình 3 ba cục than đang cháy (các cục than có kích thước như nhau).
Em hãy nhận xét về hiện tượng xảy ra trong phòng thí nghiệm?
Phương pháp giải
Dựa vào hiện tượng 3 bình trên ta thấy: 3 bình chứa lượng oxi như nhau và các cục than có kích thước như nhau => bình nào chứa ít cục than hơn sẽ cháy lâu hơn.
Hướng dẫn giải
Ở bình (1) cục than cháy lâu hơn ở bình (2). Bình (2) cục than cháy lâu hơn ở bình (3) vì lượng oxi ở 3 bình như nhau.
5. Giải bài 24.5 trang 33 SBT Hóa học 8
Người và động vật trong quá trình hô hấp hấp thụ O2, thở ra khí CO2. Nguyên liệu xăng, dầu trong quá trình đốt cháy cũng cần O2 và thải CO2. Như vậy lượng O2 phải mất dần, nhưng trong thực tế hàng nghìn năm nay, tỉ lệ về thể tích của oxi trong không khí luôn luôn xấp xỉ bằng 20%. Hãy giải thích.
Phương pháp giải
Dựa vào sự quang hợp của cây xanh để giải thích vì sao lượng O2 mất dần, nhưng trong thực tế hàng nghìn năm nay, tỉ lệ về thể tích của oxi trong không khí luôn luôn xấp xỉ bằng 20%
Hướng dẫn giải
Người và động vật trong quá trình hô hấp lấy O2, thải ra khí CO2. Nhiên liệu trong quá trình đốt cháy cũng cần O2 và thải ra CO2, nhưng lượng O2 không mất dần do sự quang hợp của cây xanh đã hấp thụ khí CO2 và tạo ra lượng khí oxi rất lớn. Do đó tỉ lệ oxi trong không khí (tính theo thể tích) luôn luôn xấp xỉ bằng 20%.
6. Giải bài 24.6 trang 33 SBT Hóa học 8
Có những chất sau: O2, Mg, P, Al, Fe. Hãy chọn một trong những chất trên và hệ số thích hợp điền vào chỗ trống trong phương trình phản ứng sau:
4Na +...\(\xrightarrow{{{t^o}}}\) 2Na2O
... + O2 \(\xrightarrow{{{t^o}}}\) 2MgO
...+ 5O2 \(\xrightarrow{{{t^o}}}\) 2P2O5
...+ 3O2 \(\xrightarrow{{{t^o}}}\) 2Al2O3
...+...\(\xrightarrow{{{t^o}}}\) Fe3O4
Phương pháp giải
Cần nắm rõ tính chất hóa học của oxi và dựa vào chất đầu và cuối để suy ra chất còn lại và viết phương trình hóa học.
Hướng dẫn giải
4Na + O2 \(\xrightarrow{{{t^o}}}\) 2Na2O
4P + 5O2 \(\xrightarrow{{{t^o}}}\) 2P2O5
4Al + 3O2 \(\xrightarrow{{{t^o}}}\) 2Al2O3
3Fe + 2O2 \(\xrightarrow{{{t^o}}}\) Fe3O4
7. Giải bài 24.7 trang 33 SBT Hóa học 8
Đổ đầy nước vào hộp cat-tông ( hộp đựng nước uống Vinamilk) kín, đun hộp đó trên bếp lửa, hộp cát-tông không cháy mà nước lại sôi.
a) Ở nhiệt độ nào thì nước sôi?
b) Trong thời gian nước sôi nhiệt độ có thay đổi không?
c) Vỏ cac-tông cháy ở nhiệt độ trên hay dưới 100oC. Tại sao?
d) Điều gì xảy ra nếu trong hộp không chứa nước?
Phương pháp giải
a) Nước sôi ở nhiệt độ 100°C .
b) Nhiệt độ không thay đổi trong thời gian nước sôi.
c) Khi trong hộp có nước vỏ các-tông không cháy, khi không có nước bên trong vỏ các-tông sẽ cháy ở nhiệt độ > 100°C.
d) Không có nước, hộp các-tông bị cháy
Hướng dẫn giải
a) Ở nhiệt độ 100°C thì nước sôi.
b) Trong thời gian nước sôi, nhiệt độ không thay đổi.
c) Vỏ các-tông không cháy trên bếp lửa khi trong hộp các-tông có đầy nước, khi trong hộp các-tông hết nước, vỏ các-tông sẽ cháy ở nhiệt độ trên 100°C.
d) Nếu trong hộp các-tông không có nước thì vỏ hộp sẽ cháy khi đun hộp trên bếp lửa.
8. Giải bài 24.8 trang 33 SBT Hóa học 8
Trong giờ học về sự cháy, một học sinh phát biểu: Cây nến cháy và bóng đèn điện cháy, phát biểu đó có đúng hay không?
Phương pháp giải
Dựa vào sự có mặt của oxi để kết luận có sự cháy ở cây nến và bóng đèn điện hay không.
Hướng dẫn giải
Phát biểu của em học sinh chỉ đúng câu đầu : Cây nến cháy vì có phản ứng cháy của nến với khí oxi, còn bóng đèn sáng lên không phải là phản ứng cháy (vì không có khí oxi) mà là dây tóc bóng đèn nóng lên thì phát sáng nhờ nguồn điện.
9. Giải bài 24.9 trang 33 SBT Hóa học 8
a) Cần bao nhiêu gam oxi để đốt cháy hoàn toàn 5 mol cacbon? 5mol lưu huỳnh?
b) Trong giờ thực hành thí nghiệm, một em học sinh đốt cháy 3,2g lưu huỳnh trong 1,12 lít oxi (đktc). Vậy theo em lưu huỳnh cháy hết hay còn dư?
Phương pháp giải
a) Phương trình hóa học
O2 → CO2
O2 → SO2
Dựa vào phương trình => Số mol oxi => Khối lượng oxi cần dùng
b) Phương trình hóa học: O2 → SO2
Tính theo phương trình hóa học => Chất dư sau phản ứng.
Hướng dẫn giải
a) O2 → CO2
5 mol5 mol
Khối lượng oxi để đốt cháy 5 mol cacbon là : 5 x 32=160(g).
O2 → SO2
5 mol5 mol
Khối lượng oxi để đốt cháy 5 mol lưu huỳnh là : 5 x 32=160(g).
b) Số mol lưu huỳnh: =0,1(mol)
Số mol oxi: = 0,05(mol)
O2 → SO2
Tỷ lệ số mol của S và O2 < 0,1/1O2 hết và S dư.
10. Giải bài 24.10 trang 33 SBT Hóa học 8
Tính thể tích khí oxi và thể tích không khí (đktc) cần thiết để đốt cháy:
a) 1mol cacbon
b) 1,5mol photpho
Cho biết oxi chiếm 20% thể tích không khí.
Phương pháp giải
a) Phương trình hóa học: O2 → CO2
b) Phương trình hóa học: + 5O2 → 2P2O5
Dựa vào phương trình => => VO2
=VO2.100.20
Hướng dẫn giải
a) Phương trình hóa học của phản ứng đốt cháy cacbon:
O2 → CO2
1 mol 1mol
Thể tích oxi (đktc) cần dùng để đốt cháy 1 mol C là: 1 x 22,4=22,4(lít).
Thể tích không khí (đktc) cần dùng để đốt cháy 1 mol C là:
×100 = 112(lit)
b) Phương trình hóa học của phản ứng đốt cháy photpho:
+ 5O2 → 2P2O5
4mol 5mol
1,5mol x mol
5×1,54=1,875(mol)
Thể tích oxi (đktc) cần dùng để đốt cháy 1,5 mol P là:
1,875 x 22,4 =42 (lít)
Thể tích không khí (đktc) cần dùng để đốt cháy 1,5 mol P là:
×100 = 210( lit)
11. Giải bài 24.11 trang 34 SBT Hóa học 8
Tính khối lượng của N/2 nguyên tử oxi, của N/4 phân tử oxi và so sánh hai kết quả này.
Phương pháp giải
= 16; MO2 = 32
Tính N/2 nguyên tử và N/4 phân tử để so sánh.
Hướng dẫn giải
Khối lượng của N nguyên tử oxi bằng 16 g
→ Khối lượng của N/2 nguyên tử oxi bằng 8 g; Khối lượng của N phân tử oxi bằng 32 g.
→ Khối lượng của N/4 phân tử oxi bằng 8 g; Hai khối lượng này giống nhau.
12. Giải bài 24.12 trang 34 SBT Hóa học 8
Đốt cháy 1 kg than trong khí oxi, biết trong than có 5% tạp chất không cháy.
a) Tính thể tích oxi(đktc) cần thiết để đốt cháy 1kg than trên.
b) Tính thể tích khí cacbonic (đktc) sinh ra trong phản ứng.
Phương pháp giải
Tính khối lượng than nguyên chất => số mol than nguyên chất
Phương trình hóa học: O2 → CO2
Dựa vào phương trình => Số mol oxi và CO2
=> Thể tích tương ứng cần tìm.
Hướng dẫn giải
Lượng than nguyên chất:
\({m_C} = \frac{{1000.95}}{{100}} = 950(g)\)
\({n_C} = \frac{{950}}{{12}} = 79,17mol\)
Ta có phương trình hóa học: C + O2 → CO2
\({n_{{O_2}}} = \frac{{79,17.1}}{1} = 79,17mol\)
a) VO2 = nO2.22,4 = 79,17.22,4 = 1773,4 (l).
b) nCO2 = nO2 = 79,17(mol) → VCO2 = VO2 = 1773,4(l)
13. Giải bài 24.13 trang 34 SBT Hóa học 8
Người ta dùng đèn xì oxi-axetilen để hàn và cắt kim loại. Phản ứng cháy axetilen C2H2 trong oxi tạo thành khí cacbonic và hơi nước. Hãy tính thể tích khí oxi (đktc) cần thiết để đốt cháy 1 mol khí axetilen.
Phương pháp giải
Phương trình hóa học:
2C2H2 + 5O2 → 4CO2 + 2H2O
Dựa vào phương trình => thể tích oxi cần dùng.
Hướng dẫn giải
Phương trình hóa học:
2C2H2 + 5O2 → 4CO2 + 2H2O
1mol 2,5mol
Thể tích oxi (đktc) dùng để đốt cháy 1 mol C2H2 là: 2,5.22,4 = 56 (lít).
14. Giải bài 24.14 trang 34 SBT Hóa học 8
Hãy cho biết 1,5.1024 phân tử oxi:
a) Là bao nhiêu mol phân tử oxi?
b) Có khối lượng là bao nhiêu gam?
c) Có thể tích là bao nhiêu lít (đktc)?
Phương pháp giải
a) 1 mol = nguyên tử hoặc phân tử chất.
b) Sử dụng công thức m= n x M (g)
c) Sử dụng công thức V= n x 22,4 (lít)
Hướng dẫn giải
a) Số mol phân tử oxi:
\(\frac{{1,{{5.10}^{24}}}}{{{{6.10}^{23}}}} = 2,5(mol)\)
b) Khối lượng của 1,5.1024 phân tử oxi:
mO2 = nO2.MO2 = 2,5.32 = 80(g)
c) Thể tích là: VO2 = nO2.22,4 = 2,5.22,4 = 56(l)
15. Giải bài 24.15 trang 34 SBT Hóa học 8
a) Trong 16(g) khí oxi có bao nhiêu mol nguyên tử oxi và bao nhiêu mol phân tử oxi?
b) Tính tỉ khối của oxi với nito, với không khí.
Phương pháp giải
a) Áp dụng công thức tính số mol: m/M(mol)
b) Áp dụng công thức tính tỉ khối: =MA/MB
Hướng dẫn giải
a) Trong 16g khí oxi có 16/16 = 1 mol nguyên tử oxi và 16/32 = 0,5 mol phân tử oxi
b) \({d_{{O_2}/N}}_{_2} = \frac{{{M_{{O_2}}}}}{{{M_{{N_2}}}}} = \frac{{32}}{{28}} = 1,14\)
\({d_{{O_2}/kk}} = \frac{{{M_{{O_2}}}}}{{29}} = \frac{{32}}{{29}} = 1,10\)
16. Giải bài 24.16 trang 34 SBT Hóa học 8
Cho 3,36 lit khí oxi (ở đktc) phản ứng hoàn toàn với 1 kim loại hóa trị III thu được 10,2g oxit. Xác định tên kim loại.
Phương pháp giải
- Bước 1: Tính số mol oxi.
- Bước 2: Phương trình hóa học: + 3O2 → 2R2O3
- Bước 3: Dựa theo phương trình hóa học ta có phương trình toán học ẩn R. Giải phương trình => Kim loại cần tìm.
Hướng dẫn giải
Gọi R là kí hiệu và nguyên tử khối của kim loại hóa trị III .
nO2 = 3,36 : 22,4 = 0,15 (mol)
Phương trình hóa học của phản ứng ;
4R + 3O2 → 2R2O3
3 mol (4R + 6 x 16) g
0,15mol 10,2 g
Theo phương trình hóa học trên, ta có :
0,15 x (4R + 6 x 16)= 10,2 x 3
→ 0,6R + 14,4 = 30,6
→ R = 27 (Al)
Vậy R là nhôm.
17. Giải bài 24.17 trang 34 SBT Hóa học 8
Để đốt cháy 1 mol chất X cần 6,5 mol O2, thu được 4 mol khí cacbonic và 5 mol nước. Xác định công thức phân tử của X.
Phương pháp giải
Áp dụng định luật bảo toàn khối lượng để xác định công thức phân tử của X.
Hướng dẫn giải
Theo đề bài, ta có phương trình hóa học:
X + 6,5O2 → 4CO2 + 5H2O
Theo định luật bảo toàn khối lượng, ta có:
1mol chất X phải có 4 mol C (4 mol CO2), 10 mol H (5 mol H2O) và không chứa oxi ( vì 2 vế của phương trình hóa học sô mol nguyên tử oxi bằng nhau).
Vậy công thức hóa học của phân tử X là C4H10.
18. Giải bài 24.18 trang 34 SBT Hóa học 8
Đốt cháy hoàn toàn 6,2 g photpho trong bình chứa 8,96 lit khi oxi (ở đktc), sản phẩm thu được là chất rắn, màu trắng. Nếu hiệu suất phản ứng là 80% thì khối lượng chất rắn thu được là bao nhiêu?
Phương pháp giải
Phương trình hóa học: 4P + 5O2 → 2P2O5
\({n_P} = \frac{{6,2}}{{31}} = 0,2mol\)
\({n_{{O_2}}} = \frac{{8,96}}{{22,4}} = 0,4mol\)
Dựa vào phương trình => chất phản ứng hết và chất dư sau phản ứng.
Số mol O5 tính theo chất phản ứng hết.
Áp dụng công thức: = (mthực tế/mlí thuyết)×100%
Hướng dẫn giải
\({n_P} = \frac{{6,2}}{{31}} = 0,2mol\)
\({n_{{O_2}}} = \frac{{8,96}}{{22,4}} = 0,4mol\)
Phương trình hóa học của phản ứng :
4P + 5O2 → 2P2O5
So sánh tỉ lệ: \(\frac{{0,2}}{{0,4}} < \frac{4}{5}\) lượng oxi dư, vậy phải tính khối lượng P2O5 theo photpho
\({n_{{P_2}{O_5}}} = \frac{{0,2.2}}{4} = 0,1mol\)
Khối lượng P2O5 thực tế thu được : 0,1.142.80% = 11,36 (g).
19. Giải bài 24.19 trang 34 SBT Hóa học 8
Đốt cháy một hỗn hợp gồm bột Fe và Mg, trong đó Mg có khối lượng 0,48g cần dùng 672ml O2 (ở đktc). Hãy tính khối lượng kim loại Fe.
Phương pháp giải
- Bước 1: Tính số mol Mg và O2
- Bước 2: Phương trình hóa học
g + O2 → 2MgO (1)
e + 2O2 → Fe3O4 (2)
- Bước 3: =1/2nMg
nO2(1)+nO2(2)= 0,03 =>nO2(2)= 0,03−nO2(1)
nFe= 32nO2(2)
=> Khối lượng Fe.
Hướng dẫn giải
\({n_{Mg}} = \frac{{0,48}}{{24}} = 0,02mol\)
\({n_{{O_2}}} = \frac{{672}}{{22400}} = 0,03mol\)
Phương trình hóa học của phản ứng :
2Mg + O2 → 2MgO
2mol 1mol
0,02mol 0,01mol
nO2 còn lại tác dụng với Fe: 0,03 - 0,01 = 0,02(mol)
3Fe + 2O2 → Fe3O4
3mol 2mol
0,03mol 0,02mol
mFe = 0,03.56 =1,68 (g)
Vậy khối lượng kim loại Fe là 1,68 (g).
Tham khảo thêm
- doc Giải bài tập SBT Hóa 8 Bài 25: Sự oxi hóa- Phản ứng hóa hợp- Ứng dụng của oxi
- doc Giải bài tập SBT Hóa 8 Bài 26: Oxit
- doc Giải bài tập SBT Hóa 8 Bài 27: Điều chế oxi- Phản ứng phân hủy
- doc Giải bài tập SBT Hóa 8 Bài 28: Không khí- Sự cháy
- doc Giải bài tập SBT Hóa 8 Bài 29: Luyện tập chương 4