Giải bài tập SBT Hóa 8 Bài 8: Luyện tập
Hướng dẫn Giải bài tập Sách bài tập Hóa học 8 Bài 8 dưới đây sẽ giúp các em học sinh nắm vững phương pháp giải bài tập và ôn luyện tốt kiến thức về nguyên tử, đơn chất, hợp chất và phân tử. Mời các em cùng theo dõi.
Mục lục nội dung
1. Giải bài 8.1 trang 9 SBT Hóa học 8
2. Giải bài 8.2 trang 10 SBT Hóa học 8
3. Giải bài 8.3 trang 10 SBT Hóa học 8
4. Giải bài 8.4 trang 10 SBT Hóa học 8
5. Giải bài 8.5 trang 10 SBT Hóa học 8
6. Giải bài 8.6 trang 11 SBT Hóa học 8
7. Giải bài 8.7 trang 11 SBT Hóa học 8

1. Giải bài 8.1 trang 9 SBT Hóa học 8
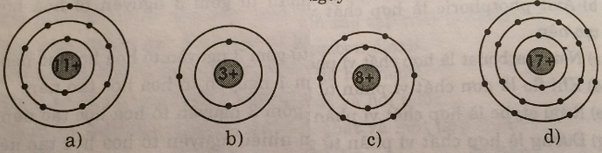
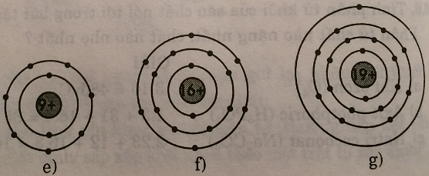
Cho biết sơ đồ nguyên tử một số nguyên tử như sau:
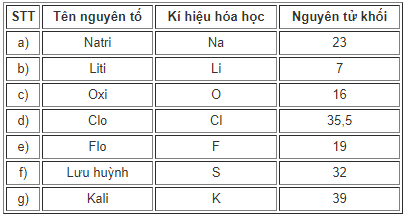
Hãy viết tên, kí hiệu hóa học và nguyên tử khối của mỗi nguyên tố (Xem bảng 1, phần phụ lục).
Phương pháp giải
Xem bảng 1 phần phụ lục SGK hóa học 8 trang 42 để trả lời câu hỏi trên.
Hướng dẫn giải
2. Giải bài 8.2 trang 10 SBT Hóa học 8
Theo sơ đồ nguyênn tử các nguyên tố cho bài 8.1, hãy chỉ ra:
Nguyên tử những nguyên tố nào có sự sắp xếp electron giống nhau về:
a, Số lớp electron (mấy lớp).
b, Số electron lớp ngoài cùng (mấy electron).
Phương pháp giải
a) 1 vòng tròn = 1 lớp e.
b) Số chấm trên vòng tròn ngoài cùng (tính từ hạt nhân) = số e lớp ngoài cùng.
Hướng dẫn giải
a) Nguyên tử các nguyên tố liti, oxi và flo giống nhau về số lớp electron, cùng có hai lớp.
Nguyên tử các nguyên tố natri, lưu huỳnh và clo giống nhau, cùng có ba lớp electron.
b) Nguyên tử các nguyên tố liti, natri và kali giống nhau về số electron ở lớp ngoài cùng, đều có 1 e.
Nguyên tử các nguyên tố clo và flo giống nhau đều có 7 e ở lớp ngoài cùng.
Nguyên tử các nguyên tố lưu huỳnh và oxi giống nhau đều có 6 e ở lớp ngoài cùng.
3. Giải bài 8.3 trang 10 SBT Hóa học 8
a) Hãy tính xem trong 1g hidro có bao nhiêu nguyên tử H ( Xem lại bài tập 7, thuộc bài học 5: Nguyên tố hóa học, SGK). Số nguyên tử H gần với con số nà nhất trong các con số cho sau đây:
A. 4.1023
B. 5.1023
C. 6.1023
D. 7.1023
b) Trong 16g oxi có số nguyên tử O bằng hay lớn hơn số nguyên tử H trên?
Phương pháp giải
Gợi ý: Cứ 1 đvC tương ứng với 1,66.10−24 g.
Hướng dẫn giải
Cứ 1 nguyên tử H có khối lượng 1,66.10-24g.
Số nguyên tử H có 1 g hidro bằng:
\(x = \frac{1}{{1,{{66.10}^{ - 24}}}} \approx 6,{02.10^{23}}\)
Đáp án C.
4. Giải bài 8.4 trang 10 SBT Hóa học 8
Hình bên là mô hình cùng sơ đồ phần tử khí amoniac (a) và khí sunfuro (b).
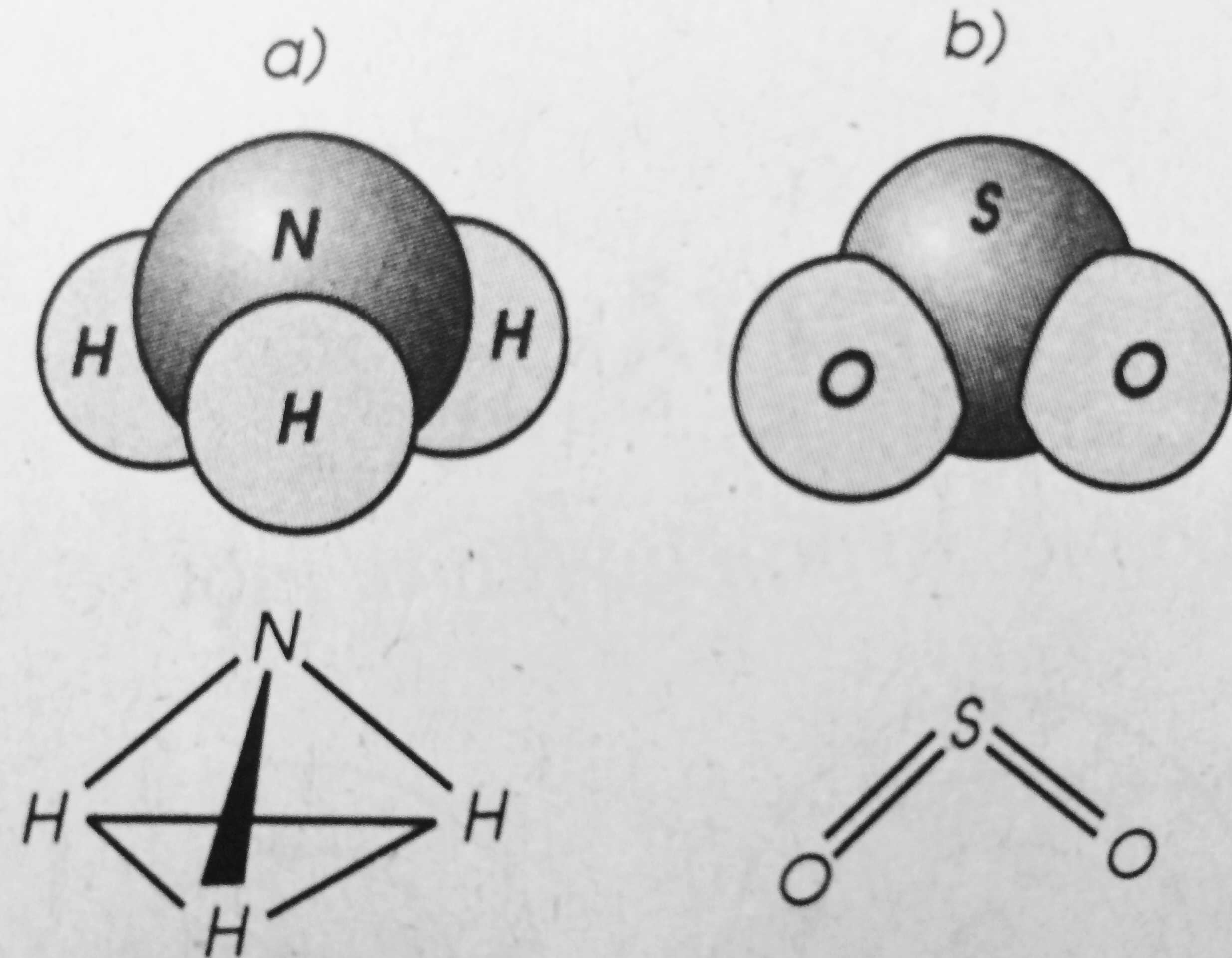
Hãy chọn các từ và con số thích hợp trong khung, điền vào chỗ trống trong đoạn câu dưới đây:
"Hai ... Đều được tạo nên từ hai ... Giống như phân tử nước, phân tử khí sunfuro hình ..., có tỉ lệ nguyên tử bằng ... Còn phân tử khí ammoniac hình ..., có tỉ lệ số nguyên tử bằng ..."
Phương pháp giải
Quan sát hình ảnh, tìm từ thích hợp điền vào chỗ trống.
Hướng dẫn giải
"Hai hợp chất đều được tạo nên từ hai nguyên tố. Giống như phân tử nước, phân tử khí sunfurơ hình gấp khúc, có tỉ lệ số nguyên tử bằng 1:2. Còn phân tử khí amoniac hình tháp tam giác, có tỉ lệ số nguyên tử bằng 1 : 3".
5. Giải bài 8.5 trang 10 SBT Hóa học 8
Phân tử một hợp chất gồm nguyên tử nguyên tố X liên kết với bốn nguyên tử H và nặng bằng nguyên tử O.
a) Tính nguyên tử khối, cho biết tên và kí hiệu hóa học của nguyên tố X.
b) Tính phần trăm về khối lượng của nguyên tố X trong hợp chất.
Phương pháp giải
a) Ta có MX + 4 MH = MO
b) Áp dụng công thức tính phần trăm khối lượng :
%mA=(x.NTK(A))/PTK(AxBy).100%
Hướng dẫn giải
a) Phân tử gồm 1X và 4H
Phân tử khối của hợp chất trên: X + 4 = 16.
Nguyên tử khối của X = 16 – 4 = 12đvC.
Vậy X là nguyên tố cacbon C
b) Phần trăm về khối lượng cacbon có trong CH4 là:
\(\% C = \frac{{12}}{{16}}.100\% = 75\% \)
6. Giải bài 8.6 trang 11 SBT Hóa học 8
Phần tử một hợp chất gồm nguyên tử nguyên tố Y liên kết với hai nguyên tử O. Nguyên tố oxi chiếm 50% về khối lượng của hợp chất.
a) Tính nguyên tử khối, cho biết tên và kí hiệu hóa học của nguyên tố Y.
b) Tính phân tử khối của hợp chất. Phân tử hợp chất nặng bằng nguyên tử nguyên tố nào?
(Xem bảng 1, phần phụ lục cuối sách).
Phương pháp giải
a) Khối lượng của 2 nguyên tử oxi là 2x 16= 32 đvC. Vì mỗi nguyên tố chiếm 50% về khối lượng.
=> Nguyên tử khối của Y là 32.
Xem bảng 1, phần phụ lục SGK hóa học 8 trang 42 để kết luận tên và KHHH của Y.
b) Phân tử khối của hợp chất bằng khối lượng của từng nguyên tố trong hợp chất .
Hướng dẫn giải
a) Khối lượng bằng đơn vị cacbon của hai nguyên tử O là : 2 X 16 = 32 (đvC)
Vì mỗi nguyên tố chiếm 50% về khối lượng nên đây cũng là khối lượng của một nguyên tử nguyên tố Y. Nguyên tử khối của Y bằng 32 đvC, Y là nguyên tố lưu huỳnh S
b) Phân tử khối của hợp chất bằng :32 + 2 . 16 = 64 (đvC)
Phân tử nặng bằng nguyên tử đồng (Cu = 64 đvC).
7. Giải bài 8.7 trang 11 SBT Hóa học 8
Dùng phễu chiết (hình bên), hãy nói cách làm để tách nước ra khỏi dầu hỏa ( dầu hôi).

Cho biết dầu hỏa là chất lỏng, có khối lượng riêng (D) khoảng 0.89g/ml và không tan trong nước.
Phương pháp giải
- Phễu chiết dùng để tách 2 chất lỏng có khối lượng riêng khác nhau và không tan vào nhau.
- Chất có khối lượng riêng nhỏ hơn (nhẹ hơn) sẽ ở phía trên, chất khối lượng riêng lớn hơn (nặng hơn) ở phía dưới. Khi mở khóa phễu chất nặng hơn sẽ chảy ra trước.
Hướng dẫn giải
Đổ hỗn hợp nước và dầu ôliu vào phễu chiết. Dầu ôliu không tan trong nước và nhẹ hơn nước nên nổi thành một lớp ở trên. Nước tách thành một lớp ở dưới. Mở phễu cho nước chảy ra từ từ đến khi hết nước thì đóng khoá phễu lại.
8. Giải bài 8.8 trang 11 SBT Hóa học 8
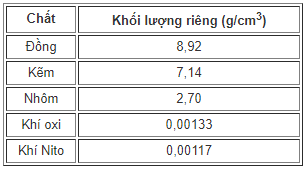
Bảng trên là khối lượng riêng của một số chất, ghi trong điều kiện thông thường.
Em có nhận xét gì về khối lượng riêng của các chất rắn so với các chất khí? Hãy giải thích vì sao?
Phương pháp giải
Cần nắm rõ lý thuyết về trạng thái chất để trả lời câu hỏi trên.
Hướng dẫn giải
Khối lượng riêng của các chất rắn lớn hơn rất nhiều (hàng nghìn lần) so với các chất khí là vì ở trạng thái khí các phân tử ở rất xa nhau, có khoảng trống rất lớn giữa các phân tử.
9. Giải bài 8.9 trang 11 SBT Hóa học 8
a) Xem lại bài tập 8.3* để biết 1 đvC tương ứng với bao nhiêu gam. Từ đó tính khối lượng bằng gam của:
• 6,02.1023 nguyên tử oxi.
• 6,02.1023 nguyên tử flo.
• 6,02.1023 nguyên tử nhôm.
Biết rằng, trong phép tính với số mũ ta có: 1024.10-24 = 1024. 1/1024 = 1
b) Nêu nhận xét về số trị của các giá trị khối lượng tính được này và số trị nguyên tử khối của mỗi nguyên tố.
Phương pháp giải
Cứ 1 đvC tương ứng với 1,66.10−24 g, tiinhs toán hoàn toàn tương tự như bài tập 8.3.
Hướng dẫn giải
a) Tính khối lượng bằng gam của:
- 6,02.1023 nguyên tử oxi: 6,02.1023.16.1,66.10-24 = 15,989 ≈ 16(g)
- 6,02.1023 nguyên tử flo: 6,02.1023.19. 1,66.10-24 = 18, 987(g) ≈ 19 (g)
- 6,02.1023 nguyên tử nhôm: 6,02.1023.19. 1,66.10-24 = 26,98(g) ≈ 27(g)
b) Số trị của các giá trị khối lượng tính được bằng chính số trị nguyên tử khối của mỗi nguyên tố.
Tham khảo thêm
- doc Giải bài tập SBT Hóa 8 Bài 2: Chất
- doc Giải bài tập SBT Hóa 8 Bài 4: Nguyên tử
- doc Giải bài tập SBT Hóa 8 Bài 5: Nguyên tố hóa học
- doc Giải bài tập SBT Hóa 8 Bài 6: Đơn chất- Hợp chất- Phân tử
- doc Giải bài tập SBT Hóa 8 Bài 9: Công thức hóa học
- doc Giải bài tập SBT Hóa 8 Bài 10: Hóa trị
- doc Giải bài tập SBT Hóa 8 Bài 11: Luyện tập chương 1