Giải bài tập SBT Hóa 8 Bài 19: Chuyển đổi giữa khối lượng, thể tích và lượng chất
Hướng dẫn Giải bài tập Sách bài tập Hóa học 8 Bài 19 dưới đây sẽ giúp các em học sinh nắm vững phương pháp giải bài tập và ôn luyện tốt kiến thức về chuyển đổi giữa khối lượng, thể tích và lượng chất . Mời các em cùng theo dõi.
Mục lục nội dung

1. Giải bài 19.1 trang 27 SBT Hóa học 8
Hãy cho biết số mol của những khối lượng chất sau:
a) 4g cacbon; 62g photpho; 42g sắt;
b) 3,6g nước; 95,48g khí cacbonnic; 14,625g muối ăn.
Phương pháp giải
Để trả lời các câu hỏi trên cần xem lại lí thuyết về sự chuyển đổi giữa khối lượng và lượng chất.
Công thức chuyển đổi giữa lượng chất (n) và khối lượng chất (m):
n = (mol)
Hướng dẫn giải
a) nC = mC : MC = 4 : 12 = 1/3 mol
nP = 62 : 31 = 2 mol
nFe = 42 : 56 = 0,75 mol
b) nH2O = 3,6 : 18 = 0,2 mol
nCO2 = 95,48 : 44 = 2,17 mol
nNaCl = 14,625 : 58,5 = 0,25 mol
2. Giải bài 19.2 trang 27 SBT Hóa học 8
Hãy tìm thể tích khí ở đktc của:
0,25 mol CO2
0,25 mol O2
21g N2
8,8g CO2
9.1023 phân tử H2
0,3.1023 phân tử CO
Phương pháp giải
Để trả lời các câu hỏi trên cần xem lại lí thuyết về sự chuyển đổi giữa khối lượng và lượng chất.
Công thức chuyển đổi giữa lượng chất (n) và thể tích của chất khí (V) ở điều kiện tiêu chuẩn
n = (mol)
Hướng dẫn giải
VCO2 = nCO2 . 22,4 = 0,25.22,4 = 5,6(l)
VO2 = nO2.22,4 = 0,25.22,4 = 5,6(l)
nN2 = 21 : 28 = 0,75 (mol)
→VN2 = nN2.22,4 = 0,75.22,4 = 16,8(lít)
nCO2 = mCO2 : MCO2 = 8,8 : 44 = 0,2 (mol)
→ VCO2 = nCO2. 22,4 = 0,2.22,4 = 4,48 (lít)
nH2 = 9.1023 : 6.1023 =1,5 (mol)
→ VH2 = nH2.22,4 = 1,5. 22,4 = 33,6(l)
nCO = (0,3.1023) : 6.1023 = 0,05(mol)
→VCO = nCO. 22,4 = 0,05. 22,4 = 1,12(l)
3. Giải bài 19.3 trang 27 SBT Hóa học 8
Vẽ biểu đồ là những hình chữ nhật để so sánh thể tích những khí sau ở đktc.
a) 1g khí hidro
b) 24g khí oxi
c) 28g khí nito
d) 88g khí cacbonic
Phương pháp giải
- Bước 1: Áp dụng công thức : m=M.n để tính số mol các chất.
- Bước 2: Tỉ lệ thể tích chính là tỉ lệ số mol => Vẽ biểu đồ.
Hướng dẫn giải
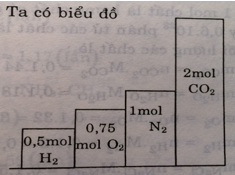
a) nH2 = 1 : 2 = 0,5 (mol)
b) nO2 = 24 : 32 = 0,75 (mol)
c) nN2 = 28 : 28 = 1 (mol)
d) nCO2= 88 : 44 = 2 (mol)
Tỉ lệ thể tích cũng chính là tỉ lệ về số mol nên ta có biểu đồ sau:
4. Giải bài 19.4 trang 27 SBT Hóa học 8
Hãy cho biết:
a) Số mol và số nguyên tử của 28g sắt (Fe); 6,4g đồng (Cu); 9g nhôm (Al).
b) Khối lượng và thể tích khí (đktc) của 2 mol H2; 1,5 mol O2; 1,15 mol CO2; 1,15 mol CH4.
Phương pháp giải
a) Áp dụng công thức m= M . n
1 mol = 6 x 1023 nguyên tử hoặc phân tử chất.
b) Áp dụng công thức m = M . n và V = 22,4 . n
Hướng dẫn giải
a) nFe = 28 : 56 = 0,5 (mol)
Số nguyên tử của Fe là: 0,5.6.1023 = 3.1023 nguyên tử hoặc 0,5N nguyên tử .
nCu = 6,4 : 64 = 0,1(mol)
Số nguyên tử của Cu là: 0,1.6.1023 = 0,6.1023 nguyên tử hoặc 0,1N nguyên tử.
nAl = 9 : 27 = 1/3 (mol)
Số nguyên tử của Al là: (1/3) . 6.1023 = 2.1023 nguyên tử hoặc 1/3.N nguyên tử.
b) mH2 = nH2.MH2 = 2.2 = 4(g) → VH2 = nH2.22,4 = 2.22,4 = 44,8(l)
mO2 = nO2.MO2 = 1,5.32 = 48(g) → VO2 = nO2.22,4 = 1,5.22,4 = 33,6(l)
mCO2 = nCO2.MCO2 = 1,15.44 = 50,6(g) → VCO2 = nCO2.22,4 = 1,15.22,4 = 25,76(l)
mCH4 = nCH4.MCH4 = 1,15.16 = 18,4(g) → VCH4 = nCH4.22,4 = 1,15.22,4 = 25,76(l)
5. Giải bài 19.5 trang 27 SBT Hóa học 8
Hãy tìm khối lượng của những đơn chất và hợp chất sau: CO2, H2O, N2, O2, H2, NaCl để cùng có số phân tử bằng nhau là 0,6.1023
Phương pháp giải
Một mol chất (đơn chất hay hợp chất) là lượng chất có chứa 6 x 1023 phân tử (hoặc nguyên tử).
Áp dụng công thức m= M . n
Hướng dẫn giải
Một mol chất (đơn chất hay hợp chất) là lượng chất có chứa 6 x 1023 phân tử (hoặc nguyên tử). Theo đề bài thì 0,6 x 1023 phân tử các chất là số phân tử có trong 0,1 mol chất. Vậy khối lượng các chất sẽ là :
mCO2 = nCO2.MCO2 = 0,1.44 = 4,4(g)
mH2O = nH2O.MH2O = 0,1.18 = 1,8(g)
mO2 = nO2.MO2 = 0,1.32 = 3,2(g)
mH2 = nH2.MH2 = 0,1.2 = 0,2(g)
mNaCl = nNaCl.MNaCl = 0,1.58,5 = 5,85(g).
6. Giải bài 19.6 trang 27 SBT Hóa học 8
Phải lấy bao nhiêu gam của mỗi chất khí sau để chúng cùng có thể tích khí là 5,6 lit ở đktc:
a) CO2
b) CH4
c) O2
d) N2
e) Cl2
Phương pháp giải
- Áp dụng công thức V= 22,4 x n => số mol của mỗi chất.
- Áp dụng công thức m = M x n => khối lượng của mỗi chất.
Hướng dẫn giải
5,6 lit khí ở đktc có số mol: n = 5,6 : 22,4 = 0,25(mol)
Để thể tích các khí đều bằng nhau là 5,6 lít (đktc) thì chúng có khối lượng:
mCO2 = nCO2.MCO2 = 0,25.44 = 11(g)
mCH4 = nCH4.MCH4 = 0,25.16 = 4(g)
mO2 = nO2.MO2 = 0,25.32 = 8(g)
mN2 = nN2.MN2 = 0,25.28 = 7(g)
mCl2 = nCl2.MCl2 = 0,25.71 = 17,75(g)