Giải bài tập SBT Hóa 9 Bài 2: Một số oxit quan trọng
Bài này sẽ giúp các em nắm vững được lý thuyết cũng như cách giải các bài tập của bài Một số oxit quan trọng với cách làm đầy đủ, chi tiết và rõ ràng. Hy vọng đây sẽ là tài liệu tham khảo hữu ích cho các em học sinh
Mục lục nội dung
1. Giải bài 2.1 trang 4 SBT Hóa học 9
2. Giải bài 2.2 trang 4 SBT Hóa học 9
3. Giải bài 2.3 trang 4 SBT Hóa học 9
4. Giải bài 2.4 trang 4 SBT Hóa học 9
5. Giải bài 2.5 trang 4 SBT Hóa học 9
6. Giải bài 2.6 trang 4 SBT Hóa học 9
7. Giải bài 2.7 trang 4 SBT Hóa học 9
8. Giải bài 2.8 trang 5 SBT Hóa học 9

1. Giải bài 2.1 trang 4 SBT Hóa học 9
Kim loại M tác dụng với dung dịch HCl sinh ra khí hiđro, dẫn khí hiđro đi qua oxit của kim loại N nung nóng. Oxit này bị khử cho kim loại N. M và N là
A. đồng và chì
B. chì và kẽm
C. kẽm và đồng
D. đồng và bạc
Phương pháp giải
Tính chất hóa học của một số oxit quan trọng.
Hướng dẫn giải
Các phương trình hoá học:
Zn + 2HCl → ZnCl2 + H2
CuO + H2 to→ Cu + H2O
Đáp án cần chọn là C
Cặp kim loại kẽm và đồng (M là Zn, N là Cu)
2. Giải bài 2.2 trang 4 SBT Hóa học 9
Canxi oxit tiếp xúc lâu ngày với không khí sẽ bị giảm chất lượng. Hãy giải thích hiện tượng này và minh hoạ bằng phương trình hoá học.
Phương pháp giải
Xem lại tính chất hóa học của CaO
- Tác dụng với nước
- Tác dụng với axit tạo thành muối và nước.
- Tác dụng với oxit axit tạo thành muối.
Hướng dẫn giải
CaO là oxit bazơ tác dụng với oxit axit CO2 trong không khí, tạo ra CaCO3 (đá vôi).
Phương trình hóa học
CaO + CO2 → CaCO3
3. Giải bài 2.3 trang 4 SBT Hóa học 9
Viết các phương trình hoá học thực hiện những chuyển đổi hoá học theo sơ đồ sau:
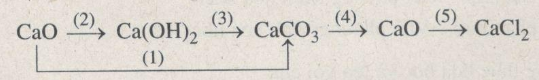
Phương pháp giải
Xem lại tính chất hóa học của một số oxit quan trọng.
Hướng dẫn giải
1. CaO + CO2 CaCO3
2. CaO + H2O Ca(OH)2
3. Ca(OH)2 + CO2 CaCO3 + H2O
4. CaCO3 to → CaO + CO2
5. CaO + 2HCl→CaCl2 + H2O
4. Giải bài 2.4 trang 4 SBT Hóa học 9
CaO là oxit bazơ, P2O5 là oxit axit. Chúng đều là những chất rắn, màu trắng. Bằng những phương pháp hoá học nào có thể giúp ta nhận biết được mỗi chất trên ?
Phương pháp giải
Dựa vào tính chất hóa học khác nhau của oxit axit và oxit bazơ.
Cho mỗi chất tác dụng với H2O, sau đó thử dung dịch bằng quỳ tím.
Hướng dẫn giải
Cho mỗi chất tác dụng với H2O, sau đó thử dung dịch bằng quỳ tím.
CaO tan trong nước tạo ra dung dịch Ca(OH)2 là dung dịch bazơ làm quỳ tím đổi sang màu xanh
P2O5 tan trong H2O tạo ra dung dịch H3PO4 là axit làm quỳ tím đổi sang màu đỏ
CaO + H2O → Ca(OH)2
P2O5 + 3H2O → 2H3PO4
5. Giải bài 2.5 trang 4 SBT Hóa học 9
Một loại đá vôi chứa 80% CaCO3. Nung 1 tấn đá vôi loại này có thể thu được bao nhiêu kg vôi sống CaO, nếu hiệu suất là 85% ?
Phương pháp giải
Tính toán theo phương trình hóa học. Chú ý đến phản ứng có hiệu suất.
Hướng dẫn giải
\({m_{CaC{O_3}}} = \dfrac{{80} }{{100}} \times 1000 = 800(kg)\)
CaCO3 to→ CaO + CO2
mCaO = 800 x 56/100 = 448(kg)
Khối lượng CaO thực tế: mCaO = 448x85/100 = 380,8 (kg)
6. Giải bài 2.6 trang 4 SBT Hóa học 9
Để tôi vôi, người ta đã dùng một khối lượng nước bằng 70% khối lượng vôi sống. Hãy cho biết khối lượng nước đã dùng lớn hơn bao nhiêu lần so với khối lượng nước tính theo phương trình hoá học.
Phương pháp giải
Vôi sống là CaO. Viết phương trình hóa học của CaO tan trong nước và tính toán.
Hướng dẫn giải
Theo phương trình hoá học: 56 kg CaO tác dụng với 18 kg H2O.
Thực tế thì khối lượng H2O dùng để tôi vôi sẽ là: 56x70/100 = 39,2(kg)
Khối lượng nước đã dùng lớn hơn là: 39,2/18 ≈ 2,2 (lần)
7. Giải bài 2.7 trang 4 SBT Hóa học 9
Cho 8 gam lưu huỳnh trioxit (SO3) tác dụng với H2O, thu được 250 ml dung dịch axit sunfuric (H2SO4)
a) Viết phương trình hoá học.
b) Xác định nồng độ mol của dung dịch axit thu được.
Phương pháp giải
Viết phương trình hóa học xảy ra và tính theo phương trình hóa học.
Hướng dẫn giải
a) Phương trình hoá học:
SO3 + H2O → H2SO4
b) Nồng độ mol của dung dịch H2SO4:
nH2SO4 = nSO3 = 8/80 = 0,1 mol
Theo phương trình hoá học:
CMdd H2SO4 = 1000x0,1/250 = 0,4M
8. Giải bài 2.8 trang 5 SBT Hóa học 9
Dẫn 1,12 lít khí lưu huỳnh đioxit (đktc) đi qua 700 ml dung dịch Ca(OH)2 0,1M.
a) Viết phương trình hoá học.
b) Tính khối lượng các chất sau phản ứng.
Phương pháp giải
Viết phương trình hóa học xảy ra và tính theo phương trình hóa học.
Hướng dẫn giải
a) Phương trình hoá học:
SO2 + Ca(OH)2 → CaSO3 + H2O
b) Khối lượng các chất sau phản ứng:
Số mol các chất đã dùng:
nSO2 = 1,12 : 22,4 = 0,05 mol; nCa(OH)2 = 0,1x700/1000 = 0,07 mol
Theo phương trình hoá học, lượng Ca(OH)2 đã dùng dư. Do đó khối lượng các chất sau phản ứng được tính theo lượng SO2.
0,05 mol SO2 tác dụng với 0,05 mol Ca(OH)2 sinh ra 0,05 mol CaSO3 và dư 0,07 - 0,05 = 0,02 (mol) Ca(OH)2.Khối lượng các chất sau phản ứng là:
mCaSO3 = 120.0,05 = 6 (gam)
mCa(OH)2 = 74.0,02 = 1,48 (gam)
9. Giải bài 2.9 trang 5 SBT Hóa học 9
Có các chất sau:
A. CuO
B H2
C. CO
D. SO3
E. P2O5
G. H2O
Hãy chọn những chất thích hợp trong các chất trên điền vào chỗ trống trong các sơ đồ phản ứng sau:
... + H2O → H2SO4
H2O + ... → H3PO4
... + HCl → CuCl2 + H2O
... + H2SO4 → CuSO4 + ...
CuO + ... to→ Cu + H2O
Phương pháp giải
Xem lại tính chất hóa học của oxit.
Hướng dẫn giải
1. SO3
2. P2O5
3. CuO
4. CuO, H2O
5. H2
10. Giải bài 2.10 trang 5 SBT Hóa học 9
Nung nóng 13,1 gam một hỗn hợp gồm Mg, Zn, Al trong không khí đến phản ứng hoàn toàn thu được 20,3 gam hỗn hợp gồm MgO, ZnO, Al2O3. Hoà tan 20,3 gam hỗn hợp oxit trên cần dùng V lít dung dịch HCl 0,4M.
a) Tính V.
b) Tính khối lượng muối clorua tạo ra.
Phương pháp giải
Viết phương trình hóa học, nhận xét mối quan hệ giữa số mol axit và nước.
Áp dụng định luật bảo toàn khối lượng để tính toán nhanh hơn.
Hướng dẫn giải
a) Ta có sơ đồ chuyển hoá:
Mg, Zn, Al → MgO, ZnO, Al2O3
MgO, ZnO, Al2O3 HCl→ MgCl2, ZnCl2, AlCl3
Ta có khối lượng O2 đã phản ứng: mO2 = 20,3 - 13,1 = 7,2 (g)
Khối lượng oxi trong H2O tạo thành khi oxit tác dụng với dung dịch HCl là 7,2 gam
⇒ nH2O = 7,2/16 = 0,45 mol
⇒ nHCl = 2nH2O = 2.0,45 = 0,9 mol
⇒ VHCl = 0,9/0,4 = 2,25l
b) Ta có: moxit + mHCl = mmuoi + mH2O
⇒ 20,3 + 0,9.36,5 = mmuoi + 0,45.18
⇒ mmuoi = 45,05g
Tham khảo thêm
- doc Giải bài tập SBT Hóa 9 Bài 1: Tính chất hóa học của oxit
- doc Giải bài tập SBT Hóa 9 Bài 3: Tính chất hóa học của axit
- doc Giải bài tập SBT Hóa 9 Bài 4: Một số axit quan trọng
- doc Giải bài tập SBT Hóa 9 Bài 5: Luyện tập: Tính chất hóa học của oxit và axit
- doc Giải bài tập SBT Hóa 9 Bài 7: Tính chất hóa học của bazơ
- doc Giải bài tập SBT Hóa 9 Bài 8: Một số bazơ quan trọng
- doc Giải bài tập SBT Hóa 9 Bài 9: Tính chất hóa học của muối
- doc Giải bài tập SBT Hóa 9 Bài 10: Một số muối quan trọng
- doc Giải bài tập SBT Hóa 9 Bài 11: Phân bón hóa học
- doc Giải bài tập SBT Hóa 9 Bài 12: Mối quan hệ giữa các loại hợp chất vô cơ
