Giải bài tập SGK Hóa 9 Bài 10: Một số muối quan trọng
Hướng dẫn Giải bài tập Hóa học 9 Bài 10 dưới đây sẽ giúp các em học sinh nắm vững phương pháp giải bài tập và ôn luyện tốt kiến thức. Mời các em cùng theo dõi.
Mục lục nội dung

1. Giải bài 1 trang 36 SGK Hóa 9
Có những muối sau: CaCO3, CaSO4, Pb(NO3)2, NaCl. Muối nào nói trên:
a) Không được phép có trong nước ăn vì tính độc hại của nó?
b) Không độc nhưng cũng không nên có trong nước ăn vì vị mặn của nó?
c) Không tan trong nước, nhưng bị phân hủy ở nhiệt độ cao?
d) Rất ít tan trong nước và khó bị phân hủy ở nhiệt độ cao?
Phương pháp giải
Để lựa chọn muối phù hợp trong mỗi trường hợp cần nắm rõ tính chất vật lý cũng như tính chất hóa học của những muối đó.
Hướng dẫn giải
Câu a
Muối không được phép có trong nước ăn vì tính độc hại của nó là Pb(NO3)2
Câu b
Muối không độc nhưng cũng không nên có trong nước ăn vì vị mặn của nó là NaCl
Câu c
Muối không tan trong nước, nhưng bị phân hủy ở nhiệt độ cao là CaCO3
Câu d
Muối rất ít tan trong nước và khó bị phân hủy ở nhiệt độ cao là CaSO4
2. Giải bài 2 trang 36 SGK Hóa 9
Hai dung dịch tác dụng với nhau, sản phẩm thu được có NaCl. Hãy cho biết hai dung dịch chất ban đầu có thể là những chất nào. Minh họa bằng các phương trình hóa học.
Phương pháp giải
Để xác định chất ban đầu ta dựa vào sản phẩm có NaCl → chất ban đầu 1 chất phải có nguyên tố Na, 1 chất phải có chứa nguyên tố Cl.
Hướng dẫn giải
Từ dung dịch ban đầu, phản ứng có sinh ra muối NaCl, suy ra một dung dịch phải là dung dịch của hợp chất có chứa Na, dung dịch còn lại là dung dịch của hợp chất có chứa Cl; Mặt khác, vì NaCl tan nên sản phẩm còn lại phải là hợp chất không tan, chất khí hay H2O, thí dụ:
- Phản ứng trung hòa HCl bằng dung dịch NaOH
NaOH + HCl → NaCl + H2O
- Phản ứng trao đổi giữa
+ Muối + axit : Na2CO3 + 2HCl → 2NaCl + CO2↑ + H2O
+ Muối + muối : BaCl2 + Na2SO4 → 2NaCl + BaSO4↓
+ Muối + kiềm : CuCl2 + 2NaOH → 2NaCl + Cu(OH)2↓
3. Giải bài 3 trang 36 SGK Hóa 9
a) Viết phương trình điện phân dung dịch muối ăn (có màng ngăn).
b) Những sản phẩm của sự điện phân dung dịch NaCl ở trên có nhiều ứng dụng quan trọng:
-Khí clo dùng để: 1)…, 2)…, 3)…
-Khí hidro dùng để:1)…, 2)…, 3)…
-Natri hiđroxit dùng để: 1)…, 2)…, 3)…
Điền những ứng dụng sau đây vào những chỗ để trống ở trên cho phù hợp:
Tẩy trắng vải, giấy; nấu xà phòng; sản xuất axit clohiđric; chế tạo hóa chất trừ sâu, diệt cỏ dại; hàn cắt kim loại; sát trùng, diệt khuẩn nước ăn; nhiên liệu cho động cơ tên lửa; bơm khí cầu, bóng thám không; sản xuất nhôm, sản xuất chất dẻo PVC; chế biến dầu mỏ.
Phương pháp giải
a) Điện phân dung dịch muối ăn (có màng ngăn) đi từ muối và nước
b) Để xác định những từ thích hợp điền vào chỗ trống cần nắm rõ ứng dụng của khí clo, khí hidro và NaOH.
Hướng dẫn giải
Câu a
Phương trình hóa học
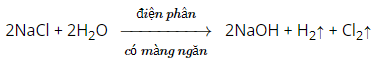
Câu b
- Khí clo dùng để: 1) tẩy trắng vải, giấy; 2) sản xuất axit HCl; 3) sản xuất chất dẻo PVC.
- Khí hiđro dùng để: 1) hàn cắt kim loại; 2) làm nhiên liệu động cơ tên lửa; 3) bơm khí cầu, bóng thám không.
- Natri hiđroxit dùng để: 1) nấu xà phòng; 2) sản xuất nhôm; 3) chế biến dầu mỏ.
4. Giải bài 4 trang 36 SGK Hóa 9
Dung dịch NaOH có thể dùng để phân biệt 2 muối có trong mỗi cặp chất sau được không? (nếu được thì ghi dấu (x), Nếu không thì ghi dấu (o) vào các ô vuông).
a) Dung dịch K2SO4 và dung dịch Fe2(SO4)3.
b) Dung dịch Na2SO4 và dung dịch CuSO4.
c) Dung dịch NaCl và dung dịch BaCl2.
Viết các phương trình hóa học, nếu có.
Phương pháp giải
Dung dịch NaOH cho vào 2 chất đó mà có hiện tượng quan sát được khác nhau thì sẽ phân biệt được.
Hướng dẫn giải
Câu a: Dung dịch K2SO4 và dung dịch Fe2(SO4)3
Khi cho dung dịch NaOH vào 2 mẫu thử gồm dung dịch K2SO4 và dung dịch Fe2(SO4)3:
- Dung dịch sau phản ứng thấy xuất hiện kết tủa nâu đỏ ⇒ Dung dịch ban đầu là Fe2(SO4)3
Fe2(SO4)3 + 6NaOH → 3Na2SO4 + 2Fe(OH)3↓
- Dung dịch còn lại là dung dịch K2SO4
Câu b: Dung dịch Na2SO4 và dung dịch CuSO4
Khi cho dung dịch NaOH vào 2 mẫu thử gồm dung dịch Na2SO4 và dung dịch CuSO4:
- Dung dịch sau phản ứng thấy xuất hiện kết tủa xanh Cu(OH)2 ⇒ Dung dịch ban đầu là dung dịch CuSO4
CuCl2 + 2NaOH → 2NaCl + Cu(OH)2↓
- Dung dịch còn lại là dung dịch Na2SO4
Câu c: Dung dịch NaCl và dung dịch BaCl2
Dung dịch NaOH không thể phân biệt được hai dung dịch trên
(Những dung dịch K2SO4, Na2SO4, NaCl, BaCl2 đều không phản ứng với dung dịch NaOH).
5. Giải bài 5 trang 36 SGK Hóa 9
Trong phòng thí nghiệm có thể dùng những muối KClO3 hoặc KNO3 để điều chế khí oxi bằng phản ứng phân hủy.
a) Viết các phương trình hóa học đối với mỗi chất.
b) Nếu dùng 0,1 mol mỗi chất thì thể tích khí oxi thu được có khác nhau hay không? Hãy tính thể tích khí oxi thu được.
c) Cần điều chế 1,12 lít khí oxi, hãy tính khối lượng mỗi chất cần dùng.
Các thể tích khí được đo ở điều kiện tiêu chuẩn?
Phương pháp giải
a) Phương trình hóa học:
2KNO3 \(\xrightarrow{{{t^o}}}\) 2KNO2 + O2↑ (1)
2KClO3 \(\xrightarrow{{{t^o}}}\) 2KCl + 3O2↑ (2)
b) Dựa vào phương trình đã viết bên trên
Đặt số mol O2 theo mol KNO3 và KClO3 từ đó tính được thể tích O2 sinh ra ở mỗi phương trình (1) ; (2)
c) Đổi số mol của O2 = 1,12/ 22,4 =?
Từ phương trình (1), (2) tính ngược lại số mol KNO3 và KClO3 từ đó tính được khối lượng của mỗi chất.
Hướng dẫn giải
Câu a
Các phương trình phản ứng phân hủy:
2KNO3 \(\xrightarrow{{{t^o}}}\) 2KNO2 + O2↑ (1)
2KClO3 \(\xrightarrow{{{t^o}}}\) 2KCl + 3O2↑ (2)
Câu b
Theo phương trình (1):
\(\\ n_{O_{2}} = \frac{1}{2} n_{KNO_{3}} = 0,05 \ mol \\ \\ V_{O_{2}} = 1,12 \ l\)
Theo phương trình (2):
\(\\ n_{O_{2}} = \frac{3}{2} n_{KClO_{3} } = 0,15 \ mol \\ \\ V_{O_{2}} = 0,15 .22,4 = 3,36 \ l\)
Câu c
\(\\ n_{O_{2}} = \frac{1,12}{22,4} =0,05 \ mol \\ \\ M_{KNO_{3}} = 101 \ g ; \ M_{KClO _{3}} = 122,5 \ g\)
nKNO3 = 0,05.2 = 0,1 mol
mKNO3 cần dùng = 0,1 . 101 = 10,1g
mKClO3 cần dùng = \(\frac{2 . 0,05 }{3 . 122,5}= 4,08 \ g\)
Vậy khối lượng mỗi chất KNO3 và KClO3 cần dùng lần lượt là 10,1 gam và 4,08 gam.
Tham khảo thêm
- docx Giải bài tập SGK Hóa 9 Bài 1: Tính chất HH của oxit và Khái quát về sự PL oxit
- docx Giải bài tập SGK Hóa 9 Bài 2: Một số oxit quan trọng
- docx Giải bài tập SGK Hóa 9 Bài 3: Tính chất hóa học của axit
- docx Giải bài tập SGK Hóa 9 Bài 4: Một số axit quan trọng
- docx Giải bài tập SGK Hóa 9 Bài 5: Luyện tập TCHH của oxit và axit
- docx Giải bài tập SGK Hóa 9 Bài 7: Tính chất hóa học của bazơ
- docx Giải bài tập SGK Hóa 9 Bài 8: Một số bazơ quan trọng
- docx Giải bài tập SGK Hóa 9 Bài 9: Tính chất hóa học của muối
- docx Giải bài tập SGK Hóa 9 Bài 11: Phân bón hóa học
- docx Giải bài tập SGK Hóa 9 Bài 12: Mối quan hệ giữa các loại hợp chất vô cơ
- docx Giải bài tập SGK Hóa 9 Bài 13: Luyện tập chương 1 Các loại hợp chất vô cơ
