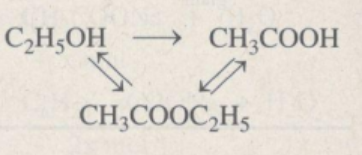Giải bài tập SBT Hóa 9 Bài 48: Luyện tập: Rượu etylic, axit axetic và chất béo
eLib giới thiệu đến các em học sinh tài liệu Giải bài tập Luyện tập môn Hóa 9. Tài liệu hướng dẫn trả lời các câu hỏi trong SBT lớp 9 môn Hóa. Mời các em tham khảo chuẩn bị tốt cho bài học sắp tới
Mục lục nội dung

1. Giải bài 48.1 trang 57 SBT Hóa học 9
Có các chất sau: C2H5OH, CH3COOH, CH3COOC2H5, (C17H35COO)3C3H5.
a) Những chất nào tan nhiều trong nước ?
b) Những chất nào có phản ứng thủy phân ?
c) Những chất nào có thể chuyển đổi trực tiếp cho nhau ?
Hãy viết các phương trình hoá học.
Phương pháp giải
Xem tính chất của một số hợp chất hữu cơ trên.
Hướng dẫn giải
a) Các chất tan nhiều trong nước: C2H5OH, CH3COOH.
b) Các chất có phản ứng thuỷ phân :
CH3COOC2H5, (C17H35COO)3C3H5.
c) Các chất chuyển đổi cho nhau theo sơ đồ
C2H5OH + O2 → CH3COOH + H2O
C2H5OH + CH3COOH → CH3COOC2H5 + H2O
2. Giải bài 48.2 trang 58 SBT Hóa học 9
Giải thích các hiện tượng sau:
a) Vào mùa đông, khi rửa bát đĩa có dính nhiều chất béo người ta thường dùng nước nóng.
b) Sau khi ép lấy dầu từ lạc người ta thường cho hơi nước nóng đi qua bã ép nhiều lần.
Phương pháp giải
Dựa vào tính tan của chất béo để giải thích.
Hướng dẫn giải
a, b: Các hiện tượng đó được giải thích dựa trên cơ sở là dầu mỡ ăn ít tan trong nước lạnh, tan nhiều hơn trong nước nóng.
3. Giải bài 48.3 trang 58 SBT Hóa học 9
Một trong các phương pháp sản xuất rượu etylic là lên men tinh bột. Phần còn lại sau khi chưng cất lấy rượu etylic gọi là bỗng rượu. Hãy giải thích tại sao bỗng rượu để trong không khí lại bị chua và khi dùng bỗng rượu để nấu canh thì lại thấy có mùi thơm.
Phương pháp giải
Trong quá trình để bỗng rượu trong không khí có thể xảy ra phản ứng hóa học nào không?
Hướng dẫn giải
Trong bỗng rượu còn một lượng nhỏ rượu (dung dịch rượu loãng). Khi để trong không khí, rượu bị chuyển thành axit axetic. Khi dùng bỗng rượu để nấu canh có một lượng nhỏ axit axetic tác dụng với rượu etylic tạo ra etyl axetat có mùi thơm
4. Giải bài 48.4 trang 58 SBT Hóa học 9
Trình bày phương pháp tách các chất ra khỏi nhau từ các hỗn hợp sau :
a) Rượu etylic và axit axetic.
b) Axit axetic và etyl axetat
Phương pháp giải
Dựa vào tính chất vật lí (nhiệt độ sôi, tính tan...) và tính chất hóa học khác nhau giữa các chất.
Hướng dẫn giải
a) Cho hỗn hợp tác dụng với CaO, sau đó chưng cất được rượu etylic. Chất rắn không bay hơi cho tác dụng với H2SO4, sau đó chưng cất thu được CH3COOH.
b) Cho hỗn hợp tác dụng với CaCO3, sau đó chưng cất được etyl axetat.
Chất rắn không bay hơi cho tác dụng với H2SO4, sau đó chưng cất thu được CH3COOH.
5. Giải bài 48.5 trang 58 SBT Hóa học 9
Tính năng lượng toả ra khi cơ thể oxi hoá hoàn toàn 15 gam chất béo. Biết 1 gam chất béo khi bị oxi hoá hoàn toàn toả ra năng lượng là 38 kJ.
Phương pháp giải
Cứ 1g chất béo khi bị oxi hóa hoàn toàn tỏa ra 38kJ
Vậy 15g chất béo khi bị oxi hóa hoàn toàn tỏa ra x kJ
→ x =?
Hướng dẫn giải
Cứ 1g chất béo khi bị oxi hóa hoàn toàn tỏa ra 38kJ
Vậy 15g chất béo khi bị oxi hóa hoàn toàn tỏa ra x kJ
→ x = 15.38/1 = 570kJ
6. Giải bài 48.6 trang 58 SBT Hóa học 9
Cho m gam hỗn hợp A gồm CH3COOH và CH3COOC2H5 tác dụng với dung dịch NaOH 1M thì vừa hết 300ml. Tách lấy toàn bộ lượng rượu etylic tạo ra rồi cho tác dụng với Na thu được 2,24 lít khí H2 (đktc).
a) Hãy viết phương trình hoá học của các phản ứng xảy ra.
b) Tính thành phần % khối lượng của mỗi chất trong hỗn hợp.
Phương pháp giải
Lập hệ phương trình 2 ẩn là số mol hai chất hữu cơ trong A dựa vào số mol NaOH và số mol H2.
Hướng dẫn giải
a) CH3COOH + NaOH → CH3COONa + H2O
CH3COOC2H5 + NaOH → CH3COONa + C2H5OH
2C2H5OH + Na → 2C2H5ONa + H2
b) Gọi số mol CH3COOH là x, số mol CH3COOC2H5 là y.
Phương trình hoá học của phản ứng giữa axit và este với NaOH :
CH3COOH + NaOH → CH3COONa + H2O
x mol x mol
CH3COOC2H5 + NaOH → CH3COONa + C2H5OH
y mol y mol y mol
Số mol NaOH phản ứng là: x + y = 300/1000 x 1 = 0,3 mol
Phương trình hoá học của phản ứng giữa rượu etylic với Na :
2C2H5OH + Na → 2C2H5ONa + H2
y y/2
Ta có y/2 = 2,24 : 22,4 = 0,1 → y = 0,2
Thay y = 0,2 vào phương trình x + y = 0,3, ta có :
x = 0,3 - 0,2 = 0,1 (mol).
Vậy khối lượng axit axetic là: 60.0,1 = 6 (gam).
Khối lượng etyl axetat là: 88.0,2 = 17,6 (gam).
Khối lượng hỗn hợp là: 6 + 17,6 = 23,6 (gam).
Vậy % khối lượng axit axetic = 6/23,6 × 100% = 25,42%
% khối lượng etyl axetat là 100% - 25,42% = 74,58%.
7. Giải bài 48.7 trang 58 SBT Hóa học 9
Đốt cháy hoàn toàn 22,2 gam một hỗn hợp gồm este có công thức CH3COOCnH2n+1 và ancol CnH2n+1OH, thu được 44 gam khí CO2 và 19,8 gam H2O. Hãy xác định công thức phân tử của este và ancol.
Phương pháp giải
Tìm số mol O trong hỗn hợp, viết phương trình hóa học, nhận xét sự chênh lệch số mol CO2 và H2O do ancol sinh ra
→ tính được số mol ancol
→ số mol O trong este
→ số mol este
→ M của ancol và este → n.
Hướng dẫn giải
Phương trình hóa học:
CH3COOCnH2n+2 + (3n+4)/2 O2 → (n+2)CO2 + (n+2)H2O
CnH2n+2OH + 3n/2O2 → nCO2 + (n+1)H2O
Áp dụng định luật bảo toàn khối lượng :
⇒ 22,2 + mO2 = 44 + 19,8 ⇒ mO2 = 41,6g
Sau phản ứng: mO = 44/44 x 32 + 19,8/18 x 16 = 49,6g
Vậy khối lượng oxi có trong este và ancol là: 49,6 - 41,6 = 8 (gam).
Theo phương trình hoá học khi đốt cháy este thu được nCO2 = nH2O còn khi đốt cháy ancol số mol H2O lớn hơn số mol CO2.
⇒ nancol = nH2O - nCO2 = 1,1 - 1 = 0,1 mol
Vậy khối lượng oxi trong este là : 8 - 16.0,1 = 6,4g
⇒ neste = 6,4 : 32 = 0,2 mol
⇒ 0,2.(n+2) + 0,1n = 1
⇒ 2n + 4 + n = 10 ⇒ n = 2
Vậy công thức phân tử của este và ancol lần lượt là CH3COOC2H5 và C2H5OH.
Tham khảo thêm
- doc Giải bài tập SBT Hóa 9 Bài 44: Rượu etylic
- doc Giải bài tập SBT Hóa 9 Bài 45: Axit axetic
- doc Giải bài tập SBT Hóa 9 Bài 46: Mối liên hệ giữa etilen, rượu etylic và axit axetic
- doc Giải bài tập SBT Hóa 9 Bài 47: Chất béo
- doc Giải bài tập SBT Hóa 9 Bài 50: Glucozơ
- doc Giải bài tập SBT Hóa 9 Bài 51: Saccarozơ
- doc Giải bài tập SBT Hóa 9 Bài 52: Tinh bột và xenlulozơ
- doc Giải bài tập SBT Hóa 9 Bài 53: Protein
- doc Giải bài tập SBT Hóa 9 Bài 54: Polime