Hoá học 8 Bài 15: Định luật bảo toàn khối lượng
Khi đốt 1Kg than thì lượng sản phẩm tạo thành có bằng 1Kg hay không? Nếu bằng mắt thường các em sẽ thấy rằng chúng không bằng nhau. Nhưng theo cơ sở khoa học thì người ta đã chứng minh bằng nhau. Như vậy chứng minh bằng cách nào? Tiết học này các em sẽ cùng nhau tìm hiểu về Định luật bảo toàn khối lượng.
Mục lục nội dung

1. Tóm tắt lý thuyết
1.1. Thí nghiệm
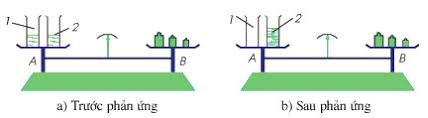
a. Cách tiến hành
Bước 1: Đặt 2 cốc chứa dd BaCl2 và Na2SO4 lên 1 đĩa cân
Bước 2: Đặt các quả cân lên đĩa cân còn lại.
Bước 3: Đổ cốc đựng dd BaCl2 vào cốc đựng dd Na2SO4.
b. Nhận xét
Kim cân ở vị trí thăng bằng.
c. Kết luận
Có chất rắn màu trắng xuất hiện gCó phản ứng hóa học xảy ra.
Kim cân ở vị trí cân bằng.
1.2. Định luật
- Trong 1 phản ứng hóa học, tổng khối lượng của các chất sản phẩm bằng tổng khối lượng của các chất tham gia phản ứng.
Phương trình chữ: A + B → C + D
Biểu thức: mA + mB = mC + mD
1.3. Áp dụng
m BariClorua + m NatriSunfat = m NatriClorua + m BariSunfat
Trong công thức này, nếu biết khối lượng của 3 chất thì ta tính được khối lượng của chất còn lại.
Gọi a, b, c lần lượt là khối lượng của Bariclorua, natrisunfat và natriclorua. Và x là số mol của Barisunfat.
Ta có: a + b = c + x
Rút giá trị x = a + b - c
2. Bài tập minh họa
2.1. Dạng 1: Tính khối lượng chất tham gia khi biết khối lượng sản phẩm
Bài 1: Đốt cháy hoàn toàn 3,1 g P trong không khí, thu được 7,1 g Điphotphopentaoxit (P2O5).
a. Viết phương trình chữ của phản ứng.
b. Tính khối lượng của oxi đã phản ứng.
Hướng dẫn giải
a. Phương trình chữ:
photpho + oxi → điphotphopentaoxit
b. Theo ĐL BTKL ta có:
m photpho + m oxi = m điphotphopentaoxit
⇒ 3,1 + m oxi = 7,1
⇒ m oxi = 7,1 - 3,1 = 4 g
Bài 2: Nung đá vôi (CaCO3) người ta thu được 112 kg Canxioxit (CaO) và 88 kg khí Cacbonic.
a. Hãy viết phương trình chữ.
b. Tính khối lượng của đá vôi cần dùng.
Hướng dẫn giải
a. Phương trình chữ:
Đá vôi → canxioxit + khí cacbonic
b. Theo ĐL BTKL ta có:
m Đá vôi = m canxioxit + m khí cacbonic
⇒ m Đá vôi = 112 + 88 = 200 kg
2.2. Dạng 2: Tính khối lượng sản phẩm
Hoà tan hoàn toàn 25,12 gam hỗn hợp 3 kim loại Mg, Al, Fe trong dung dịch HCl dư thu được 13,44 lít khí H2 (đktc) và m (gam) muối. Tính m?
Hướng dẫn giải
Sử dụng định luật bảo toàn khối lượng
nH2 = 13,44 : 22,4 =0,6 (mol) → nHCl = 2nH2 =2.0,6=1,2 (mol)
Áp dụng định luật bảo toàn khối lượng ta có:
mKl + maxit = mmuối + mH2
→ mmuối = mKl + maxit – mH2 =25,12 +1,2.36,5 – 0,6.2 = 67,72 gam
3. Luyện tập
3.1. Bài tập tự luận
Câu 1: Cho 24,4 gam hỗn hợp Na2CO3 và K2CO3 tác dụng vừa đủ với dung dịch BaCl2. Sau phản ứng thu được 39,4 gam kết tủa. Lọc tách kết tủa, cô cạn dung dịch thu được m gam muối clorua. m có giá trị là
Câu 2: Hoà tan hoàn toàn 10,14 gam hợp kim Cu, Mg, Al bằng dung dịch HCl dư thu được 7,84 lít khí A (đktc) và 1,54 gam chất rắn B và dung dịch C. Cô cạn dung dịch C thu được m gam muối. m có giá trị là
Câu 3: Trộn 5,4 gam Al với 6,0 gam Fe2O3 rồi nung nóng để thực hiện phản ứng nhiệt nhôm. Sau phản ứng ta thu được m gam hỗn hợp chất rắn. Giá trị của m là
Câu 4: Thổi một luồng khí CO dư qua ống sứ đựng m gam hỗn hợp gồm CuO, Fe2O3, FeO, Al2O3 nung nóng thu được 2,5 gam chất rắn. Toàn bộ khí thoát ra sục vào nước vôi trong dư thấy có 15 gam kết tủa trắng. Khối lượng của hỗn hợp oxit kim loại ban đầu là (biết các phản ứng xảy ra hoàn toàn)
Câu 5: Chia 1,24 gam hỗn hợp hai kim loại có hoá trị không đổi thành 2 phần bằng nhau:
– Phần 1: bị oxi hoá hoàn toàn thu được 0,78 gam hỗn hợp oxit.
– Phần 2: tan hoàn toàn trong dung dịch H2SO4 loãng thu được V lít khí H2 (đktc). Cô cạn dung dịch thu được m gam muối khan.
Giá trị của V là
3.2. Bài tập trắc nghiệm
Câu 1: Điền từ còn thiếu vào chỗ trống
“ Trong 1 phản ứng hóa học ..... khối lượng của các chất sản phẩm bằng tổng khối lượng của các chất tham gia phản ứng”
A. Tổng
B. Tích
C. Hiệu
D. Thương
Câu 2: Chon khẳng định sai
A. Sự thay đổi liên kết giữa các nguyên tử
B. Sự thay đổi liên quan đến electron
C. Sự thay đổi liên quan đến notron
D. Số nguyên tử nguyên tố được giữ nguyên
Câu 3: Chọn đáp án đúng
A. Tổng khối lượng sản phẩm bằng tổng khối lượng các chất tham gia phản ứng
B. Tổng khối lượng sản phẩm nhỏ hơn tổng khối lượng các chất tham gia phản ứng
C. Tổng khối lượng sản phẩm lớn hơn tổng khối lượng các chất tham gia phản ứng
D. Tổng khối lượng sản phẩm nhỏ hơn hoặc bằng tổng khối lượng các chất tham gia phản ứng
Câu 4: Cho 9 (g) nhôm cháy trong không khí thu được 10,2 g nhôm oxit. Tính khối lượng oxi
A. 1,7 g
B. 1,6 g
C. 1,5 g
D. 1,2 g
Câu 5: Cho sắt tác dụng với axit clohidric thu được 3, 9 g muối sắt và 7,2 g khí bay lên. Tổng khối lượn chất phản ứng
A. 11,1 g
B. 12,2 g
C. 11 g
D. 12,22
4. Kết luận
Sau bài học cần nắm:
- Quan sát thí nghiệm cụ thể, nhận xét, rút ra được kết luận về sự bảo toàn khối lượng các chất trong phản ứng hoá học
- Viết được biểu thức liên hệ giữa khối lượng các chất trong một số phản ứng cụ thể
