Giải bài tập SGK Hóa 11 Bài 13: Luyện tập: Tính chất của nitơ, photpho và hợp chất của chúng
Nội dung hướng dẫn Giải bài tập Hóa 11 Bài 13 dưới đây sẽ giúp các em học sinh nắm vững phương pháp giải bài tập và ôn luyện tốt kiến thức về tính chất của nitơ, photpho và hợp chất của chúng. Mời các em cùng theo dõi.
Mục lục nội dung
1. Giải bài 1 trang 61 SGK Hóa học 11
2. Giải bài 2 trang 61 SGK Hóa học 11
3. Giải bài 3 trang 61 SGK Hóa học 11
4. Giải bài 4 trang 61 SGK Hóa học 11
5. Giải bài 5 trang 62 SGK Hóa học 11
6. Giải bài 6 trang 62 SGK Hóa học 11
7. Giải bài 7 trang 62 SGK Hóa học 11

1. Giải bài 1 trang 61 SGK Hóa học 11
Hãy cho biết số oxi hóa của N và P trong các phân tử và ion sau đây: NH3, NH4+, NO2–, NO3–, NH4HCO3 , P2O3, PBr5, PO43–, KH2PO4, Zn3(PO4)2.
Phương pháp giải
Dựa vào quy tắc xác định số oxi hoá để tính số oxi hoá. Chú ý tổng số oxi hoá của các nguyên tử trong ion bằng điện tích của ion.
Hướng dẫn giải
Dựa vào quy tắc xác định số oxi hoá để tính số oxi hoá. Chú ý tổng số oxi hoá của các nguyên tử trong ion bằng điện tích của ion.
- Số oxi hóa của N lần lượt là: NH3 (-3), NH4+(-3), NO2– (+3), NO3– (+5), NH4HCO3 (-3)
- Số oxi hóa của P lần lượt là: P2O3 (+3), PBr5 (+5), PO43– (+5), KH2PO4 (+5), Zn3(PO4)2 (+5)
2. Giải bài 2 trang 61 SGK Hóa học 11
Trong các công thức sau đây, chọn công thức hóa học đúng của magie photphua:
A. Mg3(PO4)2
B. Mg(PO3)2
C. Mg3P2
D. Mg2P2O7
Phương pháp giải
Để chọn đáp án đúng ta cần nhớ công thức hóa học của magie photphua.
Hướng dẫn giải
Magie photphua: Mg3P2
⇒ Đáp án đúng là C.
3. Giải bài 3 trang 61 SGK Hóa học 11
a) Lập các phương trình hóa học sau đây:
NH3 + Cl2 (dư) → Na + .. (1)
NH3(dư) + Cl2 → NH4Cl + …. (2)
NH3 + CH3COOH → … (3)
(NH4)3PO4 → H3PO4 + … (4)
Zn(NO3)2 → (5)
b) Lập các phương trình hóa học ở dạng phân tử và dạng ion rút gọn của phản ứng giữa các chất sau đây trong dung dịch:
K3PO4 và Ba(NO3)2 (1)
Na3PO4 và CaCl2 (2)
Ca(H2PO4)2 và Ca(OH)2 với tỉ lệ 1:1 (3)
(NH4)3PO4 + Ba(OH)2 (4)
Phương pháp giải
Để lập phương trình hóa học ta dựa vào những chất có sẵn và tỉ lệ để suy ra những chất còn thiếu và cân bằng phương trình.
Hướng dẫn giải
Câu a: Các phương trình hóa học
(1) 2NH3 + 3Cl2 (dư) → N2 + 6HCl
(2) 8NH3(dư) + 3Cl2 → N2 + 6NH4Cl
(3) NH3 + CH3COOH → CH3COONH4
(4) (NH4)3PO4 → H3PO4 + 3NH3
(5) Zn(NO3)2 → ZnO + 2NO2 +1/2O2
Câu b: Phương trình hóa học ở dạng phân tử và dạng ion rút gọn của phản ứng
(1) 2K3PO4 + 3Ba(NO3)2 → Ba3(PO4)2 ↓+ 6KNO3
Ba2+ + 2PO43- → Ba3(PO4)2 ↓
(2) 2Na3PO4 + 3CaCl2 → Ca3(PO4)2 + 6NaCl
Ca2+ + 2PO43- → Ca3(PO4)2 ↓
(3) Ca(H2PO4)2 + Ca(OH)2 → 2CaHPO4 + 2H2O
H2PO4- + OH- → HPO42- + H2O
(4) 2(NH4)3PO4 + 3Ba(OH)2 → Ba3(PO4)2 + 6NH3 + 6H2O
6NH4+ + 2PO43- + 3Ba2+ + 6OH- → Ba3(PO4)2 ↓ + 6NH3 ↑ + 6H2O
4. Giải bài 4 trang 61 SGK Hóa học 11
Từ hiđro, clo, nitơ và các hóa chất cần thiết, hãy viết các phương trình hóa học (có ghi rõ điều kiện phản ứng) điều chế phân đạm amoni clorua.
Phương pháp giải
Để trả lời câu hỏi trên cần nắm rõ phương pháp điều chế amoni clorua.
Hướng dẫn giải
Điều chế phân đạm amoni clorua từ hiđro, clo, nitơ và các hóa chất cần thiết:
H2 + Cl2 → 2HCl
N2 + 3H2 ⇔ 2NH3
NH3 + HCl → NH4Cl
5. Giải bài 5 trang 62 SGK Hóa học 11
Viết phương trình hóa học thực hiện các dãy chuyển hóa sau đây:
a)
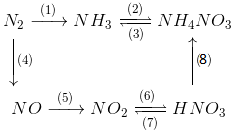
b)
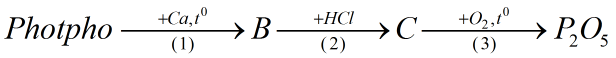
Phương pháp giải
Để viết phương trình hóa học của dãy chuyển hóa trên ta cần nắm rõ tính chất hóa học của nitơ, photpho và các hợp chất của chúng. Từ những chất có sẵn suy ra chất cần tìm.
Hướng dẫn giải
Câu a: Phương trình hóa học của dãy chuyển hóa
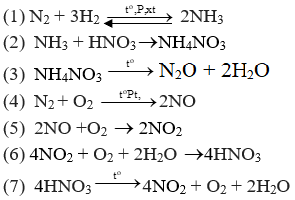
(8) NH3 + HNO3 → NH4NO3
Câu b: Phương trình hóa học của dãy chuyển hóa
(1) 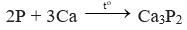
(2) Ca3P2 + 6HCl → 3CaCl2 + 2PH3
(3) 2PH3 + 4O2 → P2O5 + 3H2O
6. Giải bài 6 trang 62 SGK Hóa học 11
Hãy đưa ra những phản ứng đã học có sự tham gia của đơn chất photpho, trong đó số oxi hóa của photpho.
a) Tăng
b) Giảm
Phương pháp giải
Hướng dẫn giải
Câu a
4P + 5O2 → 2P2O5
Ở phương trình trên, photpho tăng số oxi hóa từ 0 lên +5
Câu b
2P + 3Ca → Ca3P2
Ở phương trình trên, photpho giảm số oxi hóa từ 0 xuống -3
7. Giải bài 7 trang 62 SGK Hóa học 11
Khi cho 3,00 g hỗn hợp Cu và Al tác dụng với dung dịch HNO3 đặc dư, đun nóng, sinh ra 4,48 lít khí duy nhất NO2 (đktc). Xác định phần trăm khối lượng của mỗi kim loại trong hỗn hợp?
Phương pháp giải
Hướng dẫn giải
Phương trình hóa học của phản ứng:
Cu + 4HNO3 → Cu(NO3)2 + 2NO2 + 2H2O
a 2a
Al + 6HNO3 → Al(NO3)3 + 3NO2 + 3H2O
b 3b
Ta có hệ phương trình:
\(\begin{array}{*{20}{l}} { \Rightarrow \left\{ {\begin{array}{*{20}{l}} {64a + 27b = 3\;}\\ {2a + 3b = \frac{{4,48}}{{22,4}} = 0,2} \end{array}} \right. \Leftrightarrow a = \frac{3}{{115}}}\\ { \Rightarrow \% {m_{Al}} = \frac{{3.27.100}}{{115.3}} = 23,4\% } \end{array}\)
⇒ %mCu = 76,6%
8. Giải bài 8 trang 62 SGK Hóa học 11
Cho 6,00 g P2O5 vào 25,0 ml dung dịch H3PO4 6,00% (D = 1,03 g/ml). Tính nồng độ phần trăm H3PO4 trong dung dịch tạo thành?
Phương pháp giải
Để tìm nồng độ phần trăm H3PO4 trong dung dịch ta cần tìm mH3PO4 lúc sau khi cho 6,00 g P2O5 vào 25,0 ml dung dịch H3PO4, tìm mdd mới ⇒ C%.
Hướng dẫn giải
P2O5 + 3H2O → 2H3PO4
142g → 2.98g
6g → 8,28g
\(\Rightarrow C \%_{dd \ } = \frac{(1,545+8,28).100}{6+25,75} = 30,95 \%\)
9. Giải bài 9 trang 62 SGK Hóa học 11
Cần bón bao nhiêu kg phân đạm amoni nitrat chứa 97,5% NH4NO3 cho 10,0 hecta khoai tây, biết rằng 1,00 hecta khoai tây cần 60,0 kg nitơ?
Phương pháp giải
Để tìm khối lượng phân đạm cần bón ta tìm khối lượng NH4NO3 dựa vào khối lượng nitơ.
Hướng dẫn giải
Ta có:
10 hecta cần 600 kg nitơ
Cứ 80g NH4NO3 cung cấp 28g nitơ
x kg → 600kg nitơ
x = (600.80)/28 = 1714,28 kg
Khối lượng phân đạm amoni nitrat chứa 97,5% NH4NO3:
\( \Rightarrow {m_{}} = 1714,28.\frac{{100}}{{97,5}} = 1758,24\;kg\)
Tham khảo thêm
- doc Giải bài tập SGK Hóa 11 Bài 7: Nitơ
- doc Giải bài tập SGK Hóa 11 Bài 8: Amoniac và muối amoni
- doc Giải bài tập SGK Hóa 11 Bài 9: Axit nitric và muối nitrat
- doc Giải bài tập SGK Hóa 11 Bài 10: Photpho
- doc Giải bài tập SGK Hóa 11 Bài 11: Axit photphoric và muối photphat
- doc Giải bài tập SGK Hóa 11 Bài 12: Phân bón hóa học
