Giải bài tập SGK Hóa 11 Bài 25: Ankan
Ankan có công thức cấu tạo và tính chất hóa học đặc trưng là gì? Trong thực tế ankan có ứng dụng gì ? Để biết về điều đó, eLib xin chia sẻ với các em nội dung giải bài tập SGK bên dưới đây. Với các bài tập có định hướng phương pháp và lời giải chi tiết, rõ ràng, hi vọng rằng đây sẽ là tài liệu tham khảo giúp các em học tập tốt hơn.
Mục lục nội dung

1. Giải bài 1 trang 115 SGK Hóa học 11
Thế nào là hidrocacbon no, ankan, xichoankan?
Phương pháp giải
Để giải quyết bài tập này cần nắm vững kiến thức về Hidrocacbon no, ankan và xicloankan
Hướng dẫn giải
- Hiđrocacbon no là hiđrocacbon mà trong phân tử chỉ có liên kết đơn. Hiđrocacbon no được chia thành hai loại:
+ Ankan (hay parafin) là những hiđrocacbon no không có mạch vòng.
+ Xicloankan là những hiđrocacbon no có mạch vòng.
- Hiđrocacbon no là nguồn nhiên liệu chính và là nguồn nguyên liệu quan trọng ngành công nhiệp hóa học.
2. Giải bài 2 trang 115 SGK Hóa học 11
Viết công thức phân tử của các hidrocacbon tương ứng với các gốc ankyl sau: -CH3; -C3H7; -C6H13
Phương pháp giải
Ta cộng thêm 1 H vào các gốc ankyl đó sẽ được CTPT của các hiđrocacbon tương ứng.
Hướng dẫn giải
Nhóm nguyên tử còn lại sau khi lấy bớt 1 nguyên tử H từ phân tử ankan, có công thức CnH2n+1, được gọi là nhóm ankyl.
Các hidrocacbon tương ứng: CH4; C3H8; C6H14
3. Giải bài 3 trang 115 SGK Hóa học 11
Viết các phương trình hóa học của các phản ứng sau:
a) Propan tác dụng với clo (theo tỉ lệ 1:1) khi chiếu sáng.
b) Tách một phân tử hidro từ phân tử propan.
c) Đốt cháy hexan.
Phương pháp giải
Để giải bài tập 3 cần xem lại tính chất hóa học cơ bản của ankan và các viết một số PTHH thường gặp
Hướng dẫn giải
a) C3H8 + Cl2 → C3H7Cl + HCl (điều kiện: ánh sáng)
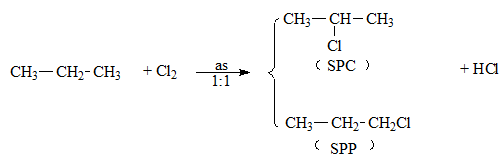
b) CH3-CH2-CH3 → CH3-CH=CH2 + H2
c) C6H14 + 19/2O2 → 6CO2 + 7H2O
4. Giải bài 4 trang 116 SGK Hóa học 11
Các hidrocacbon no được dùng làm nhiên liệu do nguyên nhân nào sau đây?
A. Hiđrocacbon no có phản ứng thế.
B. Hiđrocacbon no có nhiều trong tự nhiên.
C. Hiđrocacbon no là chất nhẹ hơn nước.
D. Hiđrocacbon no cháy tỏa nhiều nhiệt và có nhiều trong tự nhiên.
Phương pháp giải
Để giải quyết bài tập này cần nắm vững kiến thức về Hidrocacbon no
Hướng dẫn giải
Các hidrocacbon no được dùng làm nhiên liệu do hiđrocacbon no cháy tỏa nhiều nhiệt và có nhiều trong tự nhiên.
⇒ Chọn D.
5. Giải bài 5 trang 116 SGK Hóa học 11
Hãy giải thích:
a) Tại sao không được để các bình chứa xăng, dầu (gồm các ankan) gần lửa, trong khi đó người ta có thể nấu chảy nhựa đường để làm giao thông.
b) Không dùng nước để dập các đám cháy xăng, dầu mà phải dùng cát hoặc bình chứa khí cacbonic.
Phương pháp giải
Để giải quyết bài tập này cần nắm vững kiến thức về Hidrocacbon no, từ đó giải thích các hiện tượng đời sống thường gặp
Hướng dẫn giải
Câu a:
Xăng dầu gồm các ankan có mạch ngắn, dễ bay hơi, dễ bắt lửa.
Nhựa đường gồm các ankan có mạch cacbon rất lớn, khó bay hơi, kém bắt lửa.
⇒ Nên để phòng tránh cháy nổ, không được để các bình chứa xăng dầu gần lửa.
Câu b:
Vì nước không hòa tan xăng, dầu, hơn nữa xăng dầu nhẹ hơn nước nên nổi trên mặt nước và loang rộng nhanh trên bề mặt nước làm cho đám cháy lớn và rộng hơn.
Mục đích của việc dùng cát và bình chứa cacbonic là ngăn không cho xăng dầu tiếp xúc với oxi không khí. Khí cacbonic là khí không duy trì sự cháy nên đám cháy sẽ nhanh được dập tắt.
6. Giải bài 6 trang 116 SGK Hóa học 11
Công thức cấu tạo:
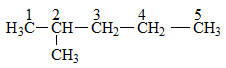
Ứng với tên gọi nào sau đây?
A. Neopentan
B. 2-metylpentan
C. Isobutan
D. 1,1-đimetylbutan
Phương pháp giải
Chọn mạch cacbon dài nhất làm mạch chính, đánh số thứ tự từ phía gần nhánh hơn
Tên ankan = số vị trí nhánh + tên mạch nhánh + tên mạch chính ( đuôi an)
Hướng dẫn giải
Công thức cấu tạo:
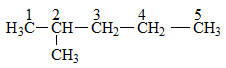
Có nhóm CH3- (metyl) ở vị trí số 2
Mạch chính gồm 5 cacbon → Pent
⇒ ứng với tên gọi 2-metylpentan
⇒ Chọn B.
7. Giải bài 7 trang 116 SGK Hóa học 11
Khi đốt cháy hoàn toàn 3,6g ankan X thu được 5,6 lít khí CO2 (đktc). Công thức phân tử của X là
A. C3H8
B. C5H10
C. C5H12
D. C4H10
Phương pháp giải
Tính được số mol CO2
Tính được khối lượng của H: mH = mX - mC
BTNT H → nH2O = 1/2nH =?
nankan = nH2O – nCO2
\(n = \frac{{{n_{CO2}}}}{{{n_X}}}\) → CTPT của X
Hướng dẫn giải
Số mol khí CO2 là:
\({n_{C{O_2}}} = \frac{{5,6}}{{22,4}} = 0,25(mol)\)
Phương trình phản ứng:
CnH2n+2 + (1,5n +0,5)O2 → nCO2 + (n +1)H2O
0,25/n ← 0,25
Ta có:
\(\frac{{3,6}}{{14n + 2}} = \frac{{0,25}}{n} \Rightarrow n = 5\)
Công thức phân tử của X là C5H12
⇒ Chọn C.
