Giải bài tập SGK Hóa 11 Bài 9: Axit nitric và muối nitrat
Nội dung hướng dẫn Giải bài tập Hóa 11 Bài 9 dưới đây sẽ giúp các em học sinh nắm vững phương pháp giải bài tập và ôn luyện tốt kiến thức về axit nitric và muối nitrat. Mời các em cùng theo dõi.
Mục lục nội dung

1. Giải bài 1 trang 45 SGK Hóa học 11
Viết công thức electron, công thức cấu tạo của axit nitric. Cho biết nguyên tố nitơ có hóa trị và số oxi hóa bao nhiêu?
Phương pháp giải
Để trả lời câu hỏi trên cần nắm công thức electron và công thức cấu tạo của axit nitric.
Hướng dẫn giải
- Công thức electron của axit nitric
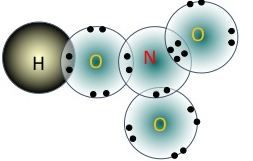
- Công thức cấu tạo phân tử

- Trong HNO3, nitơ có số oxi hóa +5 và hóa trị là 4
2. Giải bài 2 trang 45 SGK Hóa học 11
Lập các phương trình hóa học:
a) Ag + HNO3 (đặc) → NO2 + ? + ?
b) Ag + HNO3 (loãng) → NO + ? + ?
c) Al + HNO3 → N2O + ? + ?
d) Zn + HNO3 → NH4NO3 + ? + ?
e) FeO + HNO3 → NO + Fe(NO3)3 + ?
g) Fe3O4 + HNO3 → NO + Fe(NO3)3 + ?
Phương pháp giải
Trước hết, căn cứ vào tính chất, điền công thức các chất còn thiếu ở chỗ có dấu (?). Sau đó, cân bằng PTHH theo phương pháp thăng bằng electron.
Hướng dẫn giải
Câu a
Ag + 2HNO3 (đặc) → NO2 + AgNO3 + H2O
Câu b
3Ag + 4HNO3 (loãng) → NO + 3AgNO3 + 2H2O
Câu c
8Al + 30HNO3 → 3N2O + 8Al(NO3)3 + 15H2O
Câu d
4Zn + 10HNO3 → NH4NO3 + 4Zn(NO3)2 + 3H2O
Câu e
3FeO + 10HNO3 → NO + 3Fe(NO3)3 + 5H2O
Câu g
3Fe3O4 + 28HNO3 → NO + 9Fe(NO3)3 + 14H2O
3. Giải bài 3 trang 45 SGK Hóa học 11
Hãy chỉ ra những tính chất hóa học chung và khác biệt giữa axit nitric và axit sunfuric. Viết các phương trình hóa học để minh họa.
Phương pháp giải
Để chỉ ra tính chất hóa học chung của axit nitric và axit sunfuric ta cần ghi nhớ:
- Chỉ ra những tính chất chung: có tính axit mạnh.
- Tính chất riêng: HNO3 và H2SO4 đặc có tính oxi hóa mạnh.
Hướng dẫn giải
Những tính chất chung của axit nitric và axit sunfuric
- Với axit H2SO4 (loãng) và axit HNO3 đều có tính axit mạnh:
- Làm quỳ tím đổi sang màu đỏ
- Tác dụng với bazơ, oxit bazơ không có tính khử (các nguyên tố có số oxi hoá cao nhất)
2Fe(OH)2 + 3H2SO4 → Fe2(SO4)3 + 6H2O
Fe2O3 + 6HNO3 → 2Fe(HNO3)3 + 3H2O
HNO3 + CaCO3 → Ca(NO3)2 + H2O + CO2↑
H2SO4 + Na2SO3 → Na2SO4 + H2O + SO2↑
- Với axit H2SO4 (đặc) và axit HNO3 đều có tính oxi hoá mạnh
- Tác dụng được với hầu hết các kim loại (kể cả kim loại đứng sau hiđro trong dãy hoạt động hoá học) và đưa kim loại lên số oxi hoá cao nhất.
Fe + 4HNO3 → Fe(NO3)3 + NO↑ + 2H2O
Cu + 2H2SO4(đặc) → CuSO4 + SO2↑ + 2H2O
- Tác dụng với một số phi kim (đưa phi kim lên số oxi hoá cao nhất)
C + 2H2SO4(đặc) → CO2↑ + 2SO2↑ + 2H2O
S + 2HNO3 → H2SO4 + 2NO↑
- Tác dụng với hợp chất( có tính khử)
3FeO + 10HNO3 → 3Fe(NO3)3 + NO↑ + 5H2O
2Fe(OH)2 + 4H2SO4(đặc) → Fe2(SO4)3 + SO2↑ + H2O
- Cả hai axit khi làm đặc nguội đều làm Fe và Al bị thụ động hoá (có thể dùng bình làm bằng nhôm và sắt để đựng axit nitric và axit sunfuaric đặc)
Những tính chất khác biệt
- Với axit H2SO4 loãng có tính axit, còn H2SO4 đặc mới có tính oxi hoá mạnh, còn axit HNO3 dù là axit đặc hay loãng đề có tính oxi hoá mạnh khi tác dụng với các chất có tính khử.
- H2SO4 loãng không tác dụng được với các kim loại đứng sau hiđro trong dãy hoạt động hoá học như axit HNO3.
Fe + H2SO4 (loãng) → FeSO4 + H2↑
Cu + H2SO4 (loãng): không có phản ứng
4. Giải bài 4 trang 45 SGK Hóa học 11
a) Trong phương trình hóa học của phản ứng nhiệt phân sắt (III) nitrat, tổng các hệ số bằng bao nhiêu?
A. 5
B. 7
C. 9
D. 21
b) Trong phương trình hóa học của phản ứng nhiệt phân thủy ngân (II) nitrat, tổng các hệ số bằng bao nhiêu?
A. 5
B. 7
C. 9
D. 21
Phương pháp giải
Viết PTHH khi nhiệt phân 2 muối. Tính tổng hệ số của phản ứng.
Hướng dẫn giải
Câu a
Phương trình hóa học:
4Fe(NO3)3 → 2Fe2O3 + 12NO2 + 3O2
Vậy tổng hệ số là: 4 + 2 + 12 + 3 = 21
⇒ Đáp án D.
Câu b
Phương trình hóa học:
Hg(NO3)3 → Hg + 2NO2 + O2
Tổng hệ số là 1 + 1 + 2 + 1 = 5
→ Đáp án A.
5. Giải bài 5 trang 45 SGK Hóa học 11
Viết phương trình hóa học của các phản ứng thực hiện dãy chuyển hóa sau đây:
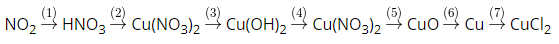
Phương pháp giải
Để viết phương trình hóa học của dãy chuyển hóa trên cần nắm rõ tính chất hóa học của đồng, axit nitric và hợp chất của chúng.
Hướng dẫn giải
Phương trình hóa học của các phản ứng:
(1) NO2 + H2O → HNO3
(2) 3Cu + 8HNO3 → 3Cu(NO3)2 + 2NO + 4H2O
(3) Cu(NO3)2 + 2NaOH → 2NaNO3 + Cu(OH)2
(4) Cu(OH)2 + 2HNO3 → Cu(NO3)2 + 2H2O
(5) 2Cu(NO3)2 → 2CuO + 4NO2 + O2
(6)
(7)
6. Giải bài 6 trang 45 SGK Hóa học 11
Khi hòa tan 30,0 g hỗn hợp đồng và đồng (II) oxit trong 1,50 lít dung dịch axit nitric 1,00 M (loãng) thấy thoát ra 6,72 lít nitơ monoaxit (đktc). Xác định hàm lượng phần trăm của đồng (II) oxit trong hỗn hợp, nồng độ mol của đồng (II) nitrat và axit nitric trong dung dịch sau phản ứng, biết rằng thể tích dung dịch không thay đổi.
Phương pháp giải
- Bước 1: Tính số mol nNO, nHNO3, viết phương trình hóa học
- Bước 2: Dựa vào phương trình tính mol của Cu, suy ra khối lượng CuO.
- Bước 3: Tính % khối lượng và nồng độ mol cần tìm.
Hướng dẫn giải
nNO= 3,72/22,4 = 0,300 (mol)
nHNO3 = 1,00 x 1,5 = 1,5 (mol)
Phương trình hóa học:
3Cu + 8HNO3 → 3Cu(NO3)2 + 2NO + 4H2O (1)
0,45 1,2 ← 0,3
nHNO3 phản ứng = 1,2 mol
Theo (1) ta tính được nCu = 0,45 mol ⇒ mCu = 28,8 gam
mCuO = 30 gam – 28,8 gam = 1,2 gam ⇒ nCuO = 0,015 mol
CuO + 2HNO3 → Cu(NO3)2 + H2O (2)
Theo (2) ta tính được nHNO3 là 0,030 mol, nCu(NO3)2 là 0,015 mol
Phần trăm khối lượng CuO:
% mCuO = \(\frac{{1,2}}{{30}}.100\% = 4\% \)
Từ (1) và (2) ta tính được số mol HNO3 dư là 0,27 mol.
Nồng độ mol HNO3 sau phản ứng: 0,27 / 1,5 = 0,18 M
Nồng độ mol của Cu(NO3)2: (0,45 + 0,015) / 1,5 = 0,31 M
7. Giải bài 7 trang 45 SGK Hóa học 11
Để điều chế 5,000 tấn axit nitric nồng độ 60,0 % cần dùng bao nhiêu tấn amoniac? Biết rằng sự hao hụt amoniac trong quá trình sản xuất là 3,8 %.
Phương pháp giải
- Bước 1: Viết phương trình hóa học, suy ra sơ đồ hợp thức.
- Bước 2: Tính khối lượng amoniac dựa vào lượng axit nitric.
Hướng dẫn giải
Các phương trình hóa học:
4NH3 + 5O2 → 4NO + 6H2O (1)
2NO + O2 → 2NO2 (2)
4NO2 + O2 + 2H2O → 4HNO3 (3)
Khối lượng HNO3 nguyên chất là: 5.60 / 100 = 3 tấn
Từ các phương trình trên ta có sơ đồ hợp thức:
NH3 → NO → NO2 → HNO3 (4)
1 mol 1 mol
17 gam 63 gam
x tấn 3 tấn
Theo sơ đồ điều chế nHNO3 = nNH3
→ mNH3 = 3.17 / 63 = 0,809524 tấn
Khối lượng NH3 hao hụt là 3,8% nghĩa là hiệu suất đạt 100 - 3,8 = 96,2%
Vậy khối lương amoniac cần dùng là: 0,809524 / 96,2% = 0,8415 tấn.
Tham khảo thêm
- doc Giải bài tập SGK Hóa 11 Bài 7: Nitơ
- doc Giải bài tập SGK Hóa 11 Bài 8: Amoniac và muối amoni
- doc Giải bài tập SGK Hóa 11 Bài 10: Photpho
- doc Giải bài tập SGK Hóa 11 Bài 11: Axit photphoric và muối photphat
- doc Giải bài tập SGK Hóa 11 Bài 12: Phân bón hóa học
- doc Giải bài tập SGK Hóa 11 Bài 13: Luyện tập: Tính chất của nitơ, photpho và hợp chất của chúng


