Giải bài tập SGK Hóa 11 Bài 42: Luyện tập Dẫn xuất halogen, ancol, phenol
Để giúp các em học sinh học tập thật tốt bộ môn Hóa học 11, eLib xin giới thiệu nội dung giải bài tập SGK bên dưới đây. Tài liệu gồm tất cả các bài tập có phương pháp và hướng dẫn giải chi tiết, rõ ràng, sẽ giúp các em ôn tập lại kiến thức, cũng cố kĩ năng làm bài hiệu quả. Mời các em cùng tham khảo.
Mục lục nội dung

1. Giải bài 1 trang 195 SGK Hóa học 11
Viết công thức cấu tạo, gọi tên các dẫn xuất halogen có công thức phân tử C4H9Cl; các ancol mạch hở có công thức phân tử C4H10O, C4H8O.
Phương pháp giải
Với dẫn xuất halogen và ancol đều có:
+ Đồng phân cấu tạo về mạch C ( mạch nhánh và mạch không phân nhánh)
+ Đồng phân về vị trí nhóm halogen hoặc ancol
- Tên gọi của dẫn xuất halogen = số chỉ vị trí nhóm halogen + tên halogen + số chỉ vị trí nhánh + tên nhánh + tên mạch chính
- Tên gọi của ancol = số chỉ vị trí nhánh + tên nhánh + tên cacbon mạch chính + số chỉ vị trí nhóm -OH + ol
Hướng dẫn giải
Các dẫn xuất halogen có CTPT C4H9Cl
CH3-CH2-CH2-CH2-Cl: 1-clobutan
CH3-CH2-CHCl-CH3: 2-clobutan
CH3-CH(CH3)-CH2-Cl: 1-clo-2metylpropan
CH3-(Cl)C(CH3)-CH3: 2-clo-2-metylpropan
Các ancol mạch hở có CTPT C4H10O
CH3-CH2-CH2-CH2-OH: butan-1-ol
CH3-CH2-CHOH-CH3: butan-2-ol
CH3-CH(CH3)-CH2-OH: 2-metylpropan-1-ol
CH3-(OH)C(CH3)-CH3: 2-metylpropan-2-ol
Các ancol mạch hở có CTPT C4H8O
CH2=CH-CH2-CH2-OH: but-3-en-2-ol
CH3-CH=CH-CH2-OH: but-2-en-1-ol
CH2=C(CH3)-CH2-OH: 2-metylpro-2en-2-ol
2. Giải bài 2 trang 195 SGK Hóa học 11
Viết phương trình hóa học của phản ứng giữa etyl bromua với: dung dịch NaOH đun nóng ; dung dịch NaOH + C2H5OH đun nóng.
Phương pháp giải
Ghi nhớ: dẫn xuất halogen phản ứng với dd NaOH trong môi trường nước thì tạo ra ancol, phản ứng với dd NaOH môi trường rượu thì tạo ra anken
→ Từ đó viết được PTHH
Hướng dẫn giải
a) C2H5Br + NaOH → C2H5OH + NaBr
b) C2H5Br + NaOH → C2H4 + NaBr + H2O
3. Giải bài 3 trang 195 SGK Hóa học 11
Viết phương trình hóa học của phản ứng giữa các ancol etylic, phenol với mỗi chất sau: natri, natri hiđroxit, nước brom, dung dịch HNO3.
Phương pháp giải
Ancol không có phản ứng với ba chất trên
Phenol có tính axit nên phản ứng được với cả 3 chất trên
Hướng dẫn giải
Phương trình hóa học của phản ứng giữa phenol với mỗi chất sau: natri hiđroxit, nước brom, dung dịch HNO3
C6H5OH + Na → C6H5ONa + H2
C6H5OH + NaOH → C6H5ONa + H2O
C6H5OH + 3Br2 → Br3C6H2OH + 3HBr
Hoặc có thể viết phương trình như sau:
.png)
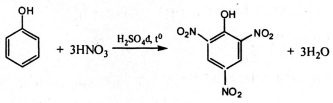
C6H5OH + HNO3 → (NO2)3C6H2OH + 3H2O
Hoặc có thể viết phương trình như sau:
Phương trình hóa học của phản ứng giữa ancol etylic với mỗi chất sau: natri hiđroxit, nước brom, dung dịch HNO3
C2H5OH + Na → C2H5ONa + H2
Ancol etylic không phản ứng với ba chất còn lại
4. Giải bài 4 trang 195 SGK Hóa học 11
Ghi Đ (đúng ) hoặc S (sai) vào ô vuông cạnh các ô sau:
a) Hợp chất C6H5- CH2-OH không thuộc loại hợp chất phenol mà thuộc ancol thơm.
b) Ancol etylic có thể hòa tan tốt phenol, nước.
c) Ancol và phenol đều có thể tác dụng với natri sinh ra khí hiđro
d) Phenol có tính axit yếu nhưng dung dịch phenol trong nước không làm đổi màu quỳ tím.
e) Phenol tan trong dung dịch NaOH là do đã phản ứng với NaOH tạo thành muối tan.
g) Phenol tan trong dung dịch NaOH chỉ là sự hòa tan bình thường .
h) Dung dịch phenol trong nước làm quỳ tím hóa đỏ.
Phương pháp giải
Xem lại tính chất hóa học của phenol, phân tích từng nhận định để xác định đúng, sai
Hướng dẫn giải
a) Đúng
b) Đúng
c) Đúng
d) Đúng
e) Đúng
g) Sai vì đây là sự hòa tan hóa học, có xảy ra phản ứng: C6H5OH + NaOH → C6H5ONa + H2O
h) Sai vì tính axit của phenol rất yếu nên không làm quỳ tím chuyển màu
5. Giải bài 5 trang 195 SGK Hóa học 11
Hoàn thành các dãy chuyển hóa sau bằng các phương trình hóa học:
a) Metan → axetilen → etilen → etanol → axit axetic
b) Benzen → brombenzen → natri phenolat → phenol → 2,4,6- tribromphenol
Phương pháp giải
Dựa vào tính chất hóa học của dẫn xuất Halogen, ancol, phenol và các dãy chuyển hóa để viết PTHH minh họa
Hướng dẫn giải
Câu a: 2CH4 (làm lạnh nhanh) → C2H2 + 3H2
C2H2 + H2 → CH2=CH2
CH2=CH2 + HOH → CH3-CH2OH
CH3-CH2OH + O2 → CH3-COOH + H2O
Câu b: Sơ đồ: C6H6 (+ Br2, Fe) → C6H5Br (+ NaOH) → C6H5ONa (+ CO2, H2O) → C6H5OH (+ Br2) → Br3C6H2OH
Phương trình hóa học:
C6H6 + Br2 → C6H5Br + HBr
C6H5Br + NaOH → C6H5ONa + NaBr + H2O
C6H5ONa + CO2 + H2O → C6H5OH + NaHCO3
.png)
6. Giải bài 6 trang 195 SGK Hóa học 11
Cho hỗn hợp gồm etanol và phenol tác dụng với natri (dư) thu được 3,36 lít khí hiđro ở đktc. Nếu cho hỗn hợp trên tác dụng với dung dịch nước brom vừa đủ thu được 19,86 gam kết tủa trắng của 2,4,6-tribromphenol
a) Viết phương trình hóa học của các phản ứng xảy ra.
b) Tính thành phần phần trăm khối lượng của mỗi chất trong hỗn hợp đã dùng.
Phương pháp giải
Khi cho tác dụng với Na thì cả phenol và natri cùng phản ứng
Còn khi tác dụng với dung dịch nước brom chỉ có mình phenol phản ứng
Từ số mol kết tủa → số mol của phenol
Từ tổng số mol của khí H2 → số mol của ancol
Hướng dẫn giải
Câu a: Gọi số mol của etanol và phenol lần lượt là x và y
Phương trình hóa học:
2C2H5OH + 2Na → 2C2H5ONa + H2
x → 0,5x
2C6H5OH + 2Na → 2C6H5ONa + H2
y → 0,5y
.png)
y → y
Câu b: Theo đề ta có hệ phương trình:
\(\left\{ \begin{array}{l}
\frac{x}{2} + \frac{y}{2} = \frac{{3,36}}{{22,4}} = 0,15\\
331y = 19,86
\end{array} \right. \Rightarrow \left\{ \begin{array}{l}
x = 0,24\\
y = 0,06
\end{array} \right.\)
Khối lượng phenol là:
mphenol = 0,06. 94,0 = 5,64 g
Khối lượng etanol là:
mC2H5OH = 0,24. 46,0 = 11,05 g
Phần trăm khối lượng của etanol là
\(\% {m_{{C_2}{H_5}OH}} = \frac{{11,04}}{{11,04 + 5,64}}.100\% = 66,2\% \)
Phần trăm khối lượng của phenol là
\(\% {m_{{C_6}{H_5}OH}} = 100 - \% {m_{{C_2}{H_5}OH}} = 100 - 66,2 = 33,8\% \)
7. Giải bài 7 trang 195 SGK Hóa học 11
Trong các chất sau, chất nào có nhiệt độ sôi cao nhất ?
A. phenol
B. etanol
C. đimetyl ete
D. metanol
Phương pháp giải
Ghi nhớ: chất có liên kết hiđro càng mạnh và phân tử khối càng lớn thì nhiệt độ sôi càng cao
Hướng dẫn giải
Phenol là chất có nhiệt độ sôi cao nhất
Đáp án A
