Giải bài tập SGK Hóa 11 Bài 17: Silic và hợp chất của silic
Nội dung hướng dẫn Giải bài tập Hóa 11 Bài 17 dưới đây sẽ giúp các em học sinh nắm vững phương pháp giải bài tập và ôn luyện tốt kiến thức về silic và hợp chất của silic. Mời các em cùng theo dõi.
Mục lục nội dung

1. Giải bài 1 trang 79 SGK Hóa học 11
Nêu những tính chất hóa học giống và khác nhau giữa silic và cacbon. Viết các phương trình hóa học để minh họa?
Phương pháp giải
Để so sánh tính chất hóa học giống và khác nhau giữa silic và cacbon ta dựa vào tính chất hóa học đặc trưng của cacbon và silic để tìm ra điểm giống và khác nhau.
Hướng dẫn giải
Những tính chất hóa học giống và khác nhau giữa silic và cacbon:
- Giống nhau: đều có các số oxi hóa -4; 0; +2; +4; vừa có tính khử, vừa có tính oxi hóa
+ Tính khử
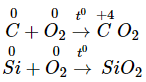
+ Tính oxi hóa
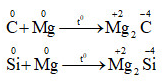
- Khác nhau:
+ Si tác dụng mạnh được với dung dịch kiềm giải phóng khí H2 còn C thì không
Si + 2NaOH + H2O → Na2SiO3 + 2H2↑
+ C khử được một số oxit kim loại còn Si thì không khử được
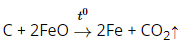
2. Giải bài 2 trang 79 SGK Hóa học 11
Số oxi hóa cao nhất của silic thể hiện ở hợp chất nào sau đây?
A. SiO
B. SiO2
C. SiH4
D. Mg2Si
Phương pháp giải
Để chọn phương án đúng ta cần xác định đúng số oxi hóa của của silic trong các hợp chất trên/
Hướng dẫn giải
Số oxi hóa cao nhất của silic thể hiện ở hợp chất SiO2 với mức oxi hóa là +4
⇒ Chọn B.
3. Giải bài 3 trang 79 SGK Hóa học 11
Khi cho nước tác dụng với oxit axit thì axit sẽ không được tạo thành, nếu oxit axit đó là
A. Cabon đioxit
B. Lưu huỳnh đioxit
C. Silic đioxit
D. Đinitơ pentaoxit
Phương pháp giải
Để chọn đáp án đúng cần nắm rõ tính chất hóa học của các oxit trên.
Hướng dẫn giải
Khi cho nước tác dụng với oxit axit thì axit sẽ không được tạo thành, nếu oxit axit đó là silic đioxit
⇒ Chọn C.
4. Giải bài 4 trang 79 SGK Hóa học 11
Từ SiO2 và các hóa chất cần thiết khác, hãy viết phương trình hóa học của các phản ứng điều chế axit silixic?
Phương pháp giải
Để viết phương trình hóa học của các phản ứng điều chế axit silixic ta cần lập sơ đồ điều chế H2SiO3 từ các chất đã cho. Căn cứ vào sơ đồ và tính chất hóa học ta viết được phương trình hóa học.
Hướng dẫn giải
Sơ đồ phản ứng:
SiO2 → NaSiO3 → H2SiO3
Các phương trình hóa học:
SiO2 + 2NaOH → Na2SiO3 + H2O
Na2SiO3 + CO2 + H2O → H2SiO3 + Na2CO3
5. Giải bài 5 trang 79 SGK Hóa học 11
Phương trình ion rút gọn: 2H+ + SiO32- → H2SiO3↓ ứng với phản ứng nào giữa các chất nào sau đây?
A. Axit cacbonic và canxi silicat.
B. Axit cacbonic và natri silicat.
C. Axit clohiđric và canxi silicat.
D. Axit clohiđric và natri silicat.
Phương pháp giải
Để chọn đáp án đúng cần nắm rõ tính chất hóa học của silic và hợ chất của silic.
Hướng dẫn giải
Phương trình ion rút gọn:
2H+ + SiO32- → H2SiO3↓ ứng với phản ứng giữa các chất axit clohiđric và natri silicat.
⇒ Chọn D.
6. Giải bài 6 trang 79 SGK Hóa học 11
Cho hỗn hợp silic và than có khối lượng 20,0 gam tác dụng với lượng dư dung dịch NaOH đặc, đun nóng. Phản ứng giải phóng ra 13,44 lít khí hiđro (đktc). Xác định thành phần phần trăm khối lượng của silic trong hỗn hợp ban đầu, biết rằng phản ứng xảy ra với hiệu suất 100%.
Phương pháp giải
Cần lưu ý: Thành phần chính của than chính là C. Khi cho Si và C tác dụng với NaOH đặc đun nóng chỉ có Si tham gia phản ứng.
Để xác định thành phần phần trăm khối lượng của silic trong hỗn hợp ta thực hiện các bước:
- Bước 1: Viết phương trình hóa học:
Si + 2NaOH đặc + H2O \(\xrightarrow{{{t^o}}}\) Na2SiO3 + 2H2↑
- Bước 2: Tính số mol Si theo số mol H2 : nSi = ½. nH2 = ? (mol)
=> khối lượng Si : mSi = nSi. MSi = ? (g)
Hướng dẫn giải
Phương trình hóa học của phản ứng:
Si + 2NaOH + 2H2O → Na2SiO3 + 2H2↑
1mol 2mol
0,30 mol 0,60 mol
%mSi = \(\frac{{0,3.28}}{{20}}.100\% \) = 42%
