Giải bài tập SGK Hóa 11 Nâng cao Bài 49: Luyện tập: Hiđrocacbon thơm với hiđrocacbon no và không no
eLib xin giới thiệu tới các em học sinh nội dung Giải bài tập SGK Hóa 11 nâng cao bài Luyện tập. Tài liệu giúp các em nắm chắc kiến thức đồng thời hướng dẫn giải các bài tập trong SGK một cách chi tiết, rõ ràng và chính xác. Hy vọng tài liệu này sẽ giúp ích cho các em học tốt môn Hóa lớp 11. Mời các em cùng tham khảo tài liệu dưới đây.
Mục lục nội dung
1. Giải bài 1 trang 207 SGK Hóa học 11 nâng cao
2. Giải bài 2 trang 207 SGK Hóa học 11 nâng cao
3. Giải bài 3 trang 207 SGK Hóa học 11 nâng cao
4. Giải bài 4 trang 207 SGK Hóa học 11 nâng cao
5. Giải bài 5 trang 207 SGK Hóa học 11 nâng cao
6. Giải bài 6 trang 207 SGK Hóa học 11 nâng cao

1. Giải bài 1 trang 207 SGK Hóa 11 nâng cao
Hãy điền những cụm từ cho dưới đây vào các chỗ trống trong các câu sau:
a) Phân tử hiđrocacbon no chỉ có các … (1) … bền vững, vì thế chúng … (2) … ở điều kiện thường. Trong phân tử … (3) … không có … (4) … đặc biệt nào, nên khi tham gia phản ứng thì thường tạo ra … (5) … sản phẩm.
A: hiđrocacbon no
B: tương đối trơ
C: liên kết δ
D: trung tâm phản ứng
b) Ở … (6) … có những … (7) …, đó là những … (8) …, chúng gây nên những … (9) … cho iđrocacbon không no.
A: trung tâm phản ứng
B: hiđrocacbon không no
C: phản ứng đặc trưng
D: liên kết π
c) Ở vòng benzen, 6 electron p tạo thành … (10) … chung, do đó bền hơn các … (11) … riêng rẽ, dẫn đến tính chất đặc trưng của … (12) … là: tương đối …(13)…, khó cộng, bền vững đối với tác nhân oxi hoá.
A: liên kết π
B: hiđrocacbon thơm
C: hệ electron π liên hợp
D: dễ thế
Phương pháp giải
Cần nắm vững kiến thức về hidrocacbon no và không no, để tìm ra câu trả lời hợp lí
Hướng dẫn giải
Câu a: Liên kết δ/ tương đối trơ/ hidrocacbon no/ trung tâm phản ứng/ nhiều.
Câu b: Hidrocacbon không no/ liên kết π/ trung tâm phản ứng/ phản ứng đặc trưng.
Câu c: Hệ electron π liên hợp/ liên kết π/ hiđrocacbon thơm/ dễ thế.
2. Giải bài 2 trang 207 SGK Hóa 11 nâng cao
Hãy viết phương trình phản ứng của toluen và naphtalen lần lượt với Cl2, Br2, HNO3, nêu rõ điều kiện phản ứng và quy tắc chi phối hướng phản ứng
Phương pháp giải
- Do ảnh hưởng của nhân thơm đối với mạch nhánh, nên khi chiếu sáng toluene tham ra phản ứng thế nguyên tử hidro ở nhóm CH3.
- Toluen tham gia phản ứng brom ở vòng dễ dàng hơn và tạo thành hỗn hợp hai đồng phân khi có xúc tác bột sắt
- Naphtalen tham gia phản ứng thế, phản ứng cộng hidro
Hướng dẫn giải
- Các phản ứng của toluen:
Cl2 + C6H5CH3 → HCl + C6H5CH2Cl
Khi có xúc tác bột Fe, Clo, brom thế vào vòng benzen
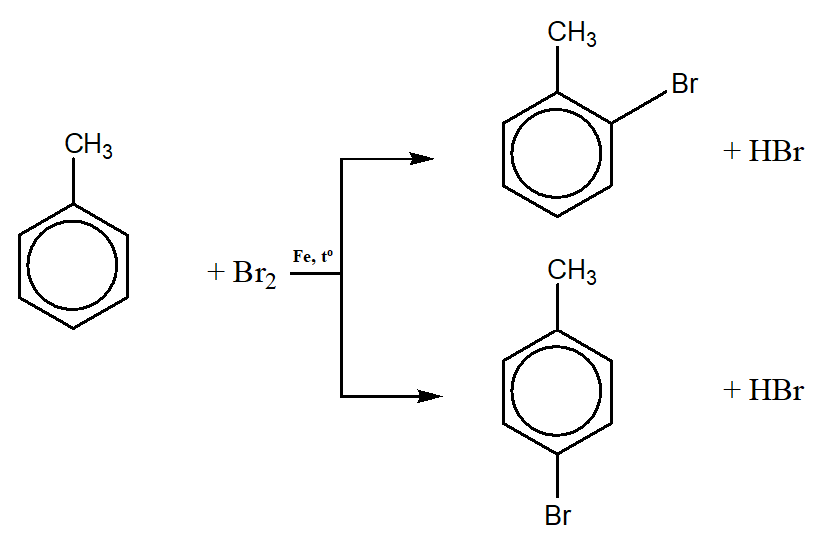
- Các phản ứng của naphtalen
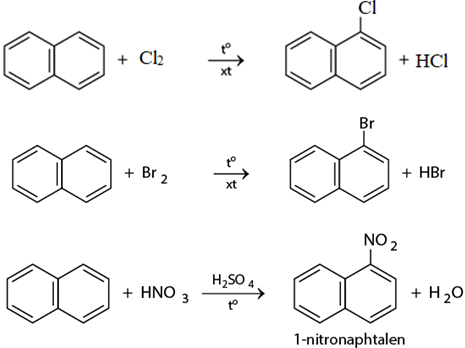
3. Giải bài 3 trang 207 SGK Hóa 11 nâng cao
Trong những chất sau: Br2, H2, HCl, H2SO4, H2O. Chất nào, trong điều kiện nào có thể cộng được vào ankylbenzen, vào anken? Viết phương trình hoá học. Cho biết quy tắc chi phối hướng của phản ứng (nếu có).
Phương pháp giải
Lưu ý
- Nếu cho các ankylbenzen phản ứng với brom trong điều kiện có bột sắt sẽ thu được hỗn hợp sản phẩm thế brom chủ yếu vào vị trí para và ortho so với nhóm ankyl:
Hướng dẫn giải
Các chất có thể phản ứng với ankylbenzen là: Br2(khan, bột sắt), H2 (Ni, to).
Các chất có thể phản ứng với anken là: Br2(dd), H2(Ni, to), HCl, H2SO4, H2O(H+, to).
Các PTHH:
- Anken
CH2=CH-CH3 + Br2 → CH2Br-CHBr-CH3
CH2=CH-CH3 + H2 → CH3-CH2-CH3
CH2=CH-CH3 + HCl → CH3-CH(Cl)-CH3
CH2=CH-CH3 + H2SO4→ CH3-CH(OSO3H)-CH3
CH2=CH-CH3 + H2O → CH3-CH(OH)-CH3
- Ankyl benzen
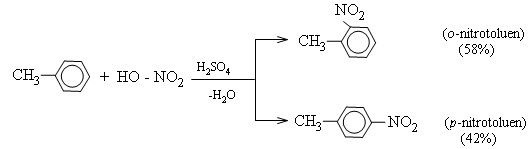
4. Giải bài 4 trang 207 SGK Hóa 11 nâng cao
Hãy dùng phương pháp hoá học phân biệt các chất trong mỗi nhóm sau:
a) Toluen, hept-1-en và heptan.
b) Etylbenzen, vinylbenzen và vinylaxetilen
Phương pháp giải
- Dùng dung dịch KMnO4
Hướng dẫn giải
Câu a: Dùng dung dịch KMnO4:
+ Chất làm mất màu thuốc tím ở điều kiện thường là hept-1-en
+ Chất làm mất màu thuốc tím khi đun nóng là toluen
+ Chất không làm mất màu thuốc tím cả khi đun nóng là heptan
Câu b: Dùng dung dịch KMnO4:
+ Các chất làm mất màu dd KMnO4 ở điều kiện thường là: vinybenzen và vinyl axetilen.
+ Chất không làm mất màu thuốc tím là etyl benzen
- Sau đó dùng AgNO3/NH3 để phân biệt vinybenzen và vinyl axetilen.
+ Chất nào có kết tủa vàng là vinyl axetilen, chất còn lại là vinybenzen.
5. Giải bài 5 trang 207 SGK Hóa 11 nâng cao
Khi cho stiren tác dụng với hiđro có Pd xúc tác ở 25oC chỉ thu được etylbenzen. Muốn thu được etylxiclohexan phải tiến hành phản ứng ở 100 – 200oC, áp suất 100atm. Hãy viết phương trình hoá học của phản ứng và giải thích.
Phương pháp giải
Vòng benzen bền nên phản ứng cộng vào vòng benzen khó khăn hơn cộng vào anken
Hướng dẫn giải
Do vòng benzen bền nên phản ứng cộng vào vòng benzen khó khăn hơn cộng vào anken nên cần tiến hành ở nhiệt độ cao hơn.
H2 + C6H5CHCH2 → C6H5CH2CH3
6. Giải bài 6 trang 207 SGK Hóa 11 nâng cao
a) Để sản xuất cumen (isopropylbenzen) người ta cho benzen phản ứng với propen có xúc tác axit, hãy viết phương trình hoá học của phản ứng.
b) Để sản xuất 1,0 tấn cumen cần dùng tối thiểu bao nhiêu m3 (đktc) hỗn hợp khí tách được từ khí crăckinh gồm 60% propen và 40% propan (về thể tích)? Biết rằng hiệu suất phản ứng đạt 80%.
c) Hãy viết phương trình hoá học của phản ứng khi cho 1mol cumen tác dụng với:
1mol brom có mặt bột Fe
1mol brom có chiếu sáng
Phương pháp giải
- Viết phương trình hóa học
- Tính nC3H6 = ncumen = ?
⇒ VC3H6 = ?
⇒ Vhh = ?
Hướng dẫn giải
Câu a: Phương trình phản ứng:
C6H6 + CH2=CH-CH3 → C6H5(CH(CH3)2)
Câu b: nC3H6 = ncumen = 106120 mol
⇒ VC3H6 = (106 : 120).22,4 ≈ 186666,7 lít ≈ 186,7m3
⇒ Vhh = (186,7.100%) : 60% ≈ 311 m3
H = 80% ⇒ Vhh = (311.100%) : 80% = 388,75m3
Câu c:
.png)
7. Giải bài 7 trang 207 SGK Hóa 11 nâng cao
Nhà máy khí Dinh Cố có 2 sản phẩm chính: khí hoá lỏng cung cấp cho thị trường và khí đốt cung cấp cho nhà máy điện Phú Mỹ.
a) Thành phần chính của mỗi sản phẩm đó là gì?
b) Có nên chuyển tất cả lượng khí khai thác được thành khí hoá lỏng hay không, vì sao?
Phương pháp giải
- Khí hóa lỏng: C3H8 và C4H10
- Khí đốt: CH4
Hướng dẫn giải
Câu a: Thành phần chính của các sản phẩm đó là:
- Khí hóa lỏng: C3H8 và C4H10
- Khí đốt: CH4
Câu b: Không nên chuyển tất cả lượng khí khai thác được thành khí hóa lỏng vì CH4 có nhiệt độ sôi rất thấp (-162oC), phải làm lạnh và nén ở áp suất cao, bình thép dùng chứa sản phẩm đó phải dày, do đó không có lợi về mặt kinh tế.
8. Giải bài 8 trang 207 SGK Hóa 11 nâng cao
Dầu mỏ hiện ta đang khai thác được chứa rất ít benzen. Em chọn phương án sản xuất benzen nào dưới đây, vì sao? Viết các phương trình hoá học của phản ứng xảy ra
a) CH4 → C2H2 → C6H6
b) Ankan C6-C7 → C6H6 + CH3C6H5 → C6H5 và CH3C6H5
Phương pháp giải
So sánh giữa 2 phương pháp ta thấy phương án b sản xuất được nhiều benzen
Hướng dẫn giải
Chọn phương án b) vì ankan có nhiều trong dầu mỏ.
PTHH:
2CH4 → C2H2 + 3H2 (làm lạnh nhanh)
3C2H2 → C6H6 (xt, to)
C6H14 → C6H6 + 4H2 (rifominh)
