Hoá học 11 Bài 22: Cấu trúc phân tử hợp chất hữu cơ
Bài giảng trình bày các nội dung cơ bản của thuyết cấu tạo hóa học: khái niệm đồng đẳng, đồng phân. Hướng dẫn cách viết công thức cấu tạo của các chất đồng phân cấu tạo và biết sơ lược về cấu trúc phân tử hợp chất hữu cơ.
Mục lục nội dung

1. Tóm tắt lý thuyết
1.1. Công thức cấu tạo
a. Khái niệm
Công thức cấu tạo biểu diễn thứ tự và cách thức liên kết (liên kết đơn, liên kết bội) của các nguyên tử trong phân tử.
Biết công thức cấu tạo của hợp chất hữu cơ sẽ dự đoán tính chất hóa học cơ bản.
b. Các loại công thức cấu tạo
Công thức cấu tạo khai triển
- Biểu diễn tất cả các liên kết trên mặt phẳng giấy.
Ví dụ:
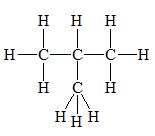
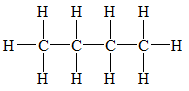
Công thức này có nhược điểm là khi viết sẽ lâu và cồng kềnh, không tiện khi viết phương trình phản ứng và tính toán hóa học do đó người ta sinh ra công thức cấu tạo thu gọn và công thức cấu tạo thu gọn nhất.
Công thức cấu tạo thu gọn
Cách biểu diễn các nguyên tử, nhóm nguyên tử cùng liên kết với một nguyên tử cacbon được viết thành một nhóm.
Ví dụ: CH3 -CH2-CH2-OH; C6H5-COOH hay CH3-CH2-CHO
Công thức cấu tạo thu gọn nhất
Cách biểu diễn chỉ biểu diễn liên kết giữa các nguyên tử cacbon và với nhóm chức. mỗi đầu đoạn thẳng hoặc điểm gấp khúc ứng với một nguyên tử cacbon, không biểu diễn số nguyên tử hiđro.
Ví dụ:
Để biểu diễn công thức cấu tạo thu gọn nhất của CH3-CH2-CH2-CH3 như sau:
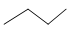
Để biểu diễn công thức cấu tạo thu gọn nhất của CH3-CH2-CH2-OH như sau:
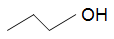
1.2. Thuyết cấu tạo hoá học
a. Nội dung
Trong phân tử hợp chất hữu cơ, các nguyên tử liên kết với nhau theo đúng hoá trị và theo một thứ tự nhất định. Thứ tự liên kết đó gọi là cấu tạo hoá học. Sự thay đổi liên kết đó tức là thay đổi cấu tạo hoá học sẽ tạo ra chất mới.
Ví dụ: Ancol etylic và đimetyl ete
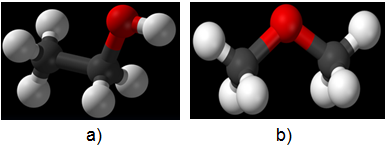
- Ancol etylic có công thức cấu tạo CH3-CH2-OH, nhiệt độ sôi ts = 78,3oC. Tan vô hạn trong nước, tác dụng với Na sinh khí H2
- Đimetyl ete có công thức cấu tạo CH3-O-CH3, nhiệt độ sôi ts = -23oC. Tan ít trong nước, không tác dụng với Na.
Trong phân tử hợp chất hữu cơ, cacbon có hoá trị bốn. Nguyên tử cacbon không những có thể liên kết với nguyên tử của các nguyên tố khác mà còn liên kết với nhau tạo thành mạch cacbon (mạch vòng, mạch không hở (mạch nhánh và mạch không nhánh)).
Mạch hở không nhánh: H3C-CH2-CH2-CH3
Mạch hở có nhánh: H3C-CH(CH3)-CH3
Mạch vòng:
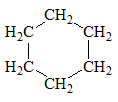
Tính chất của các chất phụ thuộc vào thành phần phân tử (bản chất, số lượng các nguyên tử) và cấu tạo hoá học (thứ tự liên kết các nguyên tử).
b. Ý nghĩa
Thuyết cấu tạo hoá học giúp giải thích được hiện tượng đồng đẳng, đồng phân.
1.3. Đồng đẳng - đồng phân
a. Đồng đẳng
Ví dụ
- Đồng đẳng của anken là:
C2H4 (CH2=CH2), C3H6 (CH2=CH-CH3), C4H8 (CH2=CH-CH2-CH3 hay CH3-CH=CH-CH3 hoặc CH2=CH(CH3)CH3) ... CnH2n
- Đồng đẳng của ancol là: CH3-OH, C2H5-OH, C3H7-OH... CnH2n+1OH
Khái niệm: Những hợp chất có thành phần phân tử hơn kém nhau một hay nhiều nhóm CH2 nhưng có tính chất hoá học tương tự nhau là những chất đồng đẳng, chúng hợp thành dãy đồng đẳng.
b. Đồng phân
Ví dụ: CH3-O-CH3 và CH3-CH2-OH đều có cùng công thức phân tử là C2H6O.
Khái niệm: Những hợp chất khác nhau nhưng có cùng công thức phân tử được gọi là các chất đồng phân của nhau.
1.4. Liên kết hóa học và cấu trúc phân tử hợp chất hữu cơ
- Gồm hai loại cơ bản là liên kết pi (π) và xichma
- Liên kết pi kém bền, liên kết xichma bền.
- Sự tổ hợp tạo ra 3 liên kết là liên kết đơn, đôi và ba.
Ví dụ về Liên kết đơn
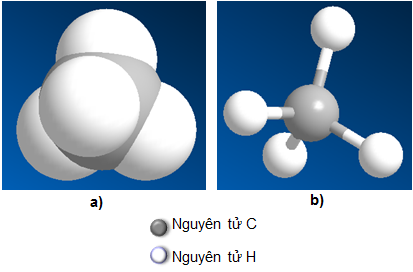
Ví dụ về Liên kết đôi
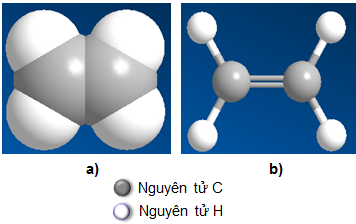
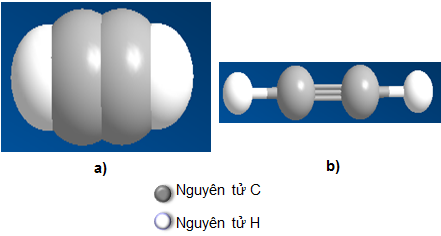
Ví dụ về Liên kết ba
2. Bài tập minh họa
2.1. Dạng 1: Cách xác định công thức hóa học hợp chất hữu cơ
Bài 1: Phân tích 0,45 gam hợp chất hữu cơ X (C, H, N), thu được 0,88 gam CO2. Mặt khác , nếu phân tích 0,45 gam X để toàn bộ N trong X chuyển thành NH3 rồi dẫn NH3 vừa tạo thành vào 100ml dung dịch H2SO4 0,4M thu được dung dịch Y. Trung hòa axit dư trong Y cần 70 ml dung dịch NaOH 1M. Biết 1 lít hơi chất X (đktc) nặng 2,009 gam. Công thức phân tử của X là
Hướng dẫn giải
nCO2 = 0,88/44 = 0,03 mol; nH2SO4 = 0,04 mol; nNaOH = 0,07 mol
2NH3 + H2SO4 → (NH4)2SO4
2NaOH + H2SO4 → Na2SO4 + 2H2O
2nH2SO4 = nNaOH + nNH3 ⇒ nNH3 = 0,01 mol
MX = 2,009.22,4 = 45
Đặt CTPT của X là CxHyNz
⇒ 0,01x = 0,02 x = 2; 0,01z = 0,01 z = 1
12.2 + y + 1.14 = 45 ⇒ y = 7 ⇒ CTPT là C7H7N
Bài 2: Đốt cháy hoàn toàn 4,4 gam hợp chất hữu cơ X ( C, H, O ). Dẫn sản phẩm cháy lần lượt qua bình (1) đựng dung dịch H2SO4 đặc, bình (2) đựng dung dịch Ca(OH)2 dư. Sau thí nghiệm, khối lượng bình (1) tăng 3,6 gam, ở bình (2) có 20 gam kết tủa. Tỉ khối của X đối với hiđro là 30. Xác định công thức của phân tử X.
Hướng dẫn giải
Đặt CTPT của X là CxHyOz
MX = 30.2 = 60 ; nCO2 = nCaCO3 = 20/100 = 0,2 mol; nH2O = 3,6/18 = 0,2 mol
nX = 6/60 = 0,1 mol
Bảo toàn nguyên tố C: 0,1.x = 0,2 ⇒ x = 2
Bảo toàn nguyên tố H: 0,1y = 2.0,2 ⇒ y = 4
12.4 + 4.1 + 16z = 60 ⇒ z = 2 ⇒ CTPT: C2H4O2
2.2. Dạng 2: Bài tập gọi tên hợp chất hữu cơ
Bài 1: Gọi tên các chất sau
a. CHCl2 - CHCl2.
b. Cl – CH2 – CH – CH – CH3
CH3 CH3
c. CH3 - CH2-Br
d. CH3 CH2-O-CH2CH3
Hướng dẫn giải
a. 1, 1, 2, 2 – tetracloetan
b. 1 - clo , 2 , 3 – đimetylbutan
c. etyl bromua
d. đietyl ete
2.3. Dạng 3: Cách viết đồng phân của hợp chất hữu cơ
Bài 1: Số công thức cấu tạo có thể có ứng với các công thức phân tử C4H10O là
Hướng dẫn giải
CH3 – CH2 – CH2 – CH2 – OH ;
CH3 – CH2 – CH(OH) - CH3;
(CH3)2CH – CH2 – OH;
(CH3)3C – OH;
CH3 – CH2 – O – CH2 – CH3;
CH3 – O – CH2 – CH2 – CH3; CH3 – O – CH(CH3)2
Bài 2: Hợp chất X có CTPT C4H8. Xác định các đông phân cấu tạo của X
Hướng dẫn giải
Ta có: Δ = (2.4+2-8)/2= 1 ⇒ có 1 lk π hoặc 1 vòng ⇒ có 2 dạng mạch cacbon:
- Mạch hở có 1 liên kết đôi trong phân tử
+ Mạch chính 4C: C-C-C-C viết được 2 TH đồng phân vị trí nối đôi:
CH2 = CH-CH2 –CH3 và CH3 - CH=CH –CH3
Mạch chính 3C: C-C(C)-C viết được 1 đồng phân
CH2=C(CH3)-CH3
- Mạch vòng và chỉ có liên kết đơn
+ Vòng 4 cạnh
+ Vòng 3 cạnh
Vậy có 5 đồng phân.
3. Luyện tập
3.1. Bài tập tự luận
Câu 1: Số công thức cấu tạo có thể có ứng với các công thức phân tử C4H9Cl là?
Câu 2:. Số công thức cấu tạo có thể có ứng với các công thức phân tử C3H6Cl2 là?
Câu 3: Số công thức cấu tạo có thể có ứng với các công thức phân tử C3H8O là?
Câu 4: Số công thức cấu tạo có thể có ứng với các công thức phân tử C4H10O là?
Câu 5: Trong số các chất : C3H8, C3H7Cl, C3H8O và C3H9N ; chất có nhiều đồng phân cấu tạo nhất là?
3.2. Bài tập trắc nghiệm
Câu 1: Chất nào sau đây trong phân tử chỉ có liên kết có liên kết đơn?
A. C2H4
B. C2H2
C. C6H6
D. C2H6.
Câu 2: Chất nào sau đây trong phân tử có liên kết đôi?
A. C2H4
B. C2H2
C. C3H8
D. C2H5OH.
Câu 3: Chất nào sau đây có phân tử có liên kết ba?
A. C2H4
B. C2H2
C. CH4
D. CH3OH.
Câu 4: Cặp chất nào sau đây là đồng phân của nhau?
A. C2H5OH, CH3OCH3
B. CH3OCH3, CH3CHO.
C. CH3OH, C2H5OH
D. CH3CH2Cl, CH3CH2OH
Câu 5: Cặp chất nào sau đây là đồng đẳng của nhau?
A. CH3OH, CH3OCH3
B. CH3OCH3, CH3CHO.
C. CH3OH, C2H5OH
D. CH3CH2OH, C3H6(OH)2.
3.3. Trắc nghiệm Online
Các em hãy luyện tập bài trắc nghiệm Cấu trúc phân tử hợp chất hữu cơ Hóa học 11 sau để nắm rõ thêm kiến thức bài học.
4. Kết luận
Sau bài học cần nắm:
- Khái niệm đồng đẳng, đồng phân.
- Cách viết công thức cấu tạo của các chất đồng phân cấu tạo
- Sơ lược về cấu trúc phân tử hợp chất hữu cơ.
