Hoá học 11 Bài 36: Luyện tập Hiđrocacbon thơm
Nội dung Bài Luyện tập Hiđrocacbon thơm giúp HS biết được những điểm giống nhau và khác nhau về tính chất hóa học của các hiđrocacbon thơm với các ankan, anken, tính chất hóa học của các hiđrocacbon thơm.
Mục lục nội dung

1. Tóm tắt lý thuyết
1.1. Danh pháp
a. Hệ thống
Số chỉ vị trí của nhóm ankyl + tên ankyl + benzen.
Tổng số chỉ vị trí: nhỏ nhất.
Tên ankyl: gọi theo bảng chữ cái.
b. Thay thế
1,2 thay bằng ortho
1,3 thay bằng meta
1,4 thay bằng para
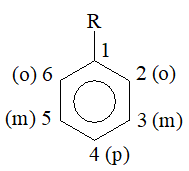
Với R: nhóm ankyl
c. Thông thường
toluen, các xilen
1.2. Tính chất hóa học
a. Phản ứng thế
(thế nguyên tử hiđro)
Nhánh (ankyl): nhiệt độ. Vd: Brom khan.
Vòng: bột sắt.
Vd: halogen, axitric.
Quy tắc thế: Các ankyl benzen dễ tham gia phản ứng thế nguyên tử hiđro của vòng benzen hơn benzen và sự thế ưu tiên ở vị trí ortho và para so với nhóm ankyl.
b. Phản ứng cộng
Nhánh (có liên kết đôi, ba): dung dịch Br2, HBr, H2O.
Vòng: tạo vòng no: Hiđro.
c. Phản ứng oxi hóa
Hoàn toàn: phản ứng cháy.
Không hoàn toàn: ( phản ứng với dung dịch KMnO4 )
Vòng: không tác dụng. Bền với tác nhân oxi hóa là dung dịch KMnO4.
Nhánh:
No (ankyl): nhiệt độ cao.
Không no: nhiệt độ thường.
2. Bài tập minh họa
2.1. Dạng 1: Phản ứng thế ( Clo hóa; brom hóa, nitro hóa)
Bài 1: TNT (2,4,6- trinitrotoluen) được điều chế bằng phản ứng của toluen với hỗn hợp gồm HNO3 đặc và H2SO4 đặc, trong điều kiện đun nóng. Biết hiệu suất của toàn bộ quá trình tổng hợp là 80%. Lượng TNT (2,4,6- trinitrotoluen) tạo thành từ 230 gam toluen là
A. 550,0 gam.
B. 687,5 gam.
C. 454,0 gam.
D. 567,5 gam.
Hướng dẫn giải
C6H5CH3 + 3HNO3 → C6H2(NO2)3CH3 + 3H2O
92 227
230 x
Theo phương trình và giả thiết ta thấy khối lượng TNT (2,4,6-trinitrotoluen) tạo thành từ 230 gam toluen với hiệu suất 80% là :
x = 230.227/92.80% =454gam.
⇒ Đáp án C
2.2. Dạng 2: Phản ứng oxi hóa
Để oxi hoá hết 10,6 gam o-xylen (1,2-đimetylbenzen) cần bao nhiêu lít dung dịch KMnO4 0,5M trong môi trường H2SO4 loãng. Giả sử dùng dư 20% so với lượng phản ứng.
A. 0,48 lít.
B. 0,24 lít.
C. 0,12 lít.
D. 0,576 lít.
Hướng dẫn giải
Phương trình phản ứng :
5H3C-C6H4-CH3+12KMnO4+18H2SO4 → 5HOOC-C6H4-COOH + 6K2SO4+12MnSO4 +28H2O
nKMnO4 = 12/5.n o-xylen = 0,24 mol
⇒ nKMnO4 dùng = 0,24 + 0,24.20% = 0,288mol
Vdd KMnO4 = 0,288 : 0,5 = 0,576 (mol)
⇒ Đáp án D
Có thể dùng phương pháp bảo toàn e:
Mn+7 + 5e → Mn+2
2C-3 → 2C+3 + 12e
5nKMnO4 = 12no-xylen
2.3. Dạng 3: Trùng hợp stiren
Bài 1: Đem trùng hợp 5,2 gam stiren hỗn hợp sau phản ứng cho tác dụng với 100ml dd Br2 0,15 M sau đó tiếp tục cho thêm KI dư vào thì được 0,635 gam iot . Khối lượng polime tạo thành là:
A. 5,2g
B. 3,9
C.3,64g
D. 4,16g
Hướng dẫn giải
nI2= 0,0025 (mol)
nBr2= 0,015 (mol)
do Br2 dư tác dụng với
2KI + Br2→2KBr + I2
0,0025 0,0025
nBr2 pư với Stiren= 0,015 – 0,0025= 0,0125 (mol)
(C6H5) - CH=CH2 + Br2 → (C6H5) – CH(Br ) - CH2-Br
0,0125 ← 0,0125 (mol)
mstiren dư tác dụng với Br2 = 0,0125 . 104= 1,3 (g)
m stiren trùng hợp = 5,2- 1,3 = 3,9 (g) = mpolime
Bài 2: Tiến hành trùng hợp 20,8 gam stiren. Hỗn hợp thu được sau phản ứng tác dụng vừa đủ với 500ml dung dịch Br2 0,2M. Phần trăm stiren đã tham gia phản ứng trùng hợp là:
A. 25%.
B. 50%.
C. 60%.
D. 75%.
Hướng dẫn giải
nBr2 = nstiren dư =0,2.0,5 = 0,1 mol
mstiren dư = 0,1.104 = 10,4g ⇒ mstiren trùng hợp = 20,8 – 10,4 = 10,4g
%mstiren trùng hợp = (10,4 )/20,8 .100% = 50%
⇒ Đáp án B
3. Luyện tập
3.1. Bài tập tự luận
Câu 1: Xét một số nhóm thế trên vòng benzen: -CH3; -NH3Cl; -OCH3; -NO2; -COOH; -Cl và -SO3H. Hãy cho biết trong số này có bao nhiêu nhóm định thế vòng benzen ở vị trí meta?
Câu 2: Cho 39 gam benzen vào 100 gam HNO3 63% sau đó thêm axit H2SO4 đặc vào và đun nóng. Tính khối lượng nitrobenzen thu được nếu hiệu suất của phản ứng đạt 80%.
Câu 3: Đốt cháy hoàn toàn 2,9 gam hỗn hợp X gồm hai hiđrocacbon kế tiếp nhau trong dãy đồng đẳng của benzen thu được 9,68 gam CO2. Vậy công thức của 2 aren là:
Câu 4: Cho toluen tác dụng với lượng dư HNO3 đặc có xúc tác H2SO4 đặc để điều chế 2,4,6-trinitrotoluen (TNT). KHối lượng điều chế được từ 23 kg toluen (hiệu suất 80%) là?
3.2. Bài tập trắc nghiệm
Câu 1: Toluen tác dụng với dung dịch KMnO4 khi đun nóng, thu được sản phẩm hữu cơ là
A. C6H5OK.
B. C6H5CH2OH.
C. C6H5CHO.
D. C6H5COOK.
Câu 2: Hiđrocacbon X không làm mất màu dung dịch brom ở nhiệt độ thường. X là chất nào sau đây?
A. benzen
B. etilen
C. propen
D. stiren.
Câu 3: Sản phẩm chủ yếu trong hỗn hợp thu được khi cho toluen phản ứng với brom theo tỷ lệ mol 1 : 1 (có một bột sắt) là
A. Benzybromua.
B. o-bromtoluen và p-bromtoluen.
C. p-bromtoluen và m-bromtoluen.
D. o-bromtoluen và m-bromtoluen.
Câu 4: Cho các chất axetilen, vinyl axetilen, stiren, toluen, hexan, benzen. Trong các chất trên, số chất phản ứng được với brom là:
A.3
B. 4
C. 5
D. 2.
Câu 5: Để phân biệt toluen, benzen, stiren chỉ cần dùng dung dịch
A.NaOH
B. HCl
C. Br2
D. KMnO4
3.3. Trắc nghiệm Online
Các em hãy luyện tập bài trắc nghiệm Luyện tập Hiđrocacbon thơm Hóa học 11 sau để nắm rõ thêm kiến thức bài học.
4. Kết luận
Sau bài học cần nắm:
- Những điểm giống nhau và khác nhau về tính chất hóa học của các hiđrocacbon thơm với các ankan, anken.
- Tính chất hóa học của các hiđrocacbon thơm.
