Hoá học 9 Bài 46: Mối liên hệ giữa etilen, rượu etylic và axit axetic
Các em đã học Hidrocacbon, rượu, axit. Vậy các hợp chất trên có mối liên hệ với nhau như thế nào? Chúng có thể chuyển đổi qua lại hay không? Chúng ta cùng nhau tìm hiểu qua bài giảng Mối liên hệ giữa etilen, rượu etylic và axit axetic.
Mục lục nội dung

1. Tóm tắt lý thuyết
1.1. Mối liên hệ giữa etilen, rượu etylic và axit axetic
a) Cấu trúc của Etilen, Rượu etylic và Axit axetic
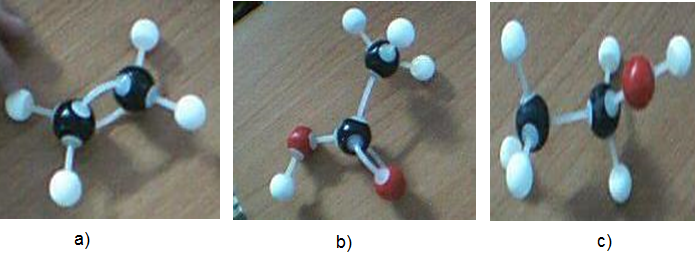
a) Etilen b) Rượu etylic c) Axit axetic
b) Sơ đồ mối liên hệ giữa các chất

Ví dụ: Hoàn thành chuỗi phản ứng sau: C2H4 \(\overset{(1)}{\rightarrow}\) C2H5OH \(\overset{(2)}{\rightarrow}\) CH3COOH \(\overset{(3)}{\rightarrow}\) CH3COOC2H5
Phương trình phản ứng:
(1) C2H4(k) + H2O(l) \(\overset{Axit}{\rightarrow}\) C2H5OH
(2) C2H5OH + O2 \(\overset{men giam}{\rightarrow}\) CH3COOH + H2O
(3) C2H5OH + CH3COOH .png) CH3COOC2H5 + H2O
CH3COOC2H5 + H2O
1.2. Tổng kết
2. Bài tập minh họa
2.1. Dạng 1: Bài tập nhận biết
Chỉ dùng H2O và một hoá chất, hãy phân biệt các chất sau: Rượu etylic, axit axetic, etyl axetat.
Hướng dẫn giải
- Dùng quỳ tím nhận ra CH3COOH. Mẫu nào làm quỳ tím chuyển đỏ là axit axetic, còn lại là rượu etylic và etylaxetat
- Dùng H2O nhận ra rượu etylic (tan trong nước), chất còn lại không tan trong nước là etyl axetat.
2.2. Dạng 2: Hiệu suất của phản ứng
Cho 22,4 lít khí etilen (ở điều kiện tiêu chuẩn) tác dụng với nước có axit sunfuric làm xúc tác, thu được 13,8 gam rượu etylic. Hãy tính hiệu suất phản ứng cộng nước của etilen.
Hướng dẫn giải
Số mol khí etilen là: \({n_{{C_2}{H_4}}} = \frac{{22,4}}{{22,4}} = 1(mol)\)
Phương trình phản ứng :
C2H4(k) + H2O(l) \(\overset{Axit}{\rightarrow}\) C2H5OH
1(mol) → 1 (mol)
Khối lượng rượu etylic thu được theo lí thuyết là: 1. 46 = 46 (gam)
Ta có khối lượng rượu etylic thu được thực tế là 13,8 gam
Hiệu suất của phản ứng công nước của etilen là: \(H = \frac{{{m_{tt}}}}{{{m_{lt}}}}.100 = \frac{{13,8}}{{46}}.100 = 30\%\)
2.3. Dạng 3. Xác định công thức phân tử
Đốt cháy 23 gam chất hữu cơ A thu được sản phẩm gồm 44 gam CO2 và 27 gam H2O:
a) Hỏi trong A có những nguyên tố nào.
b) Xác định công thức phân tử của A, biết tỉ khối hơi của A so với hiđro là 23.
Hướng dẫn giải
a) Đốt cháy A thu được CO2 và H2O. Vậy A chứa nguyên tố cacbon, hiđro và có thể có nguyên tố oxi.
\(\begin{array}{*{20}{l}}
{{m_C} = {n_{C{O_2}}}.{M_C} = \frac{{44}}{{44}}.12 = 12\;g}\\
{\;{m_H} = 2.{n_{{H_2}O}} = 2.\frac{{27}}{{18}} = 3\;g}
\end{array}\)
\({m_O} = {m_A} - ({m_C} + {m_H})=23-(12+3)=8(gam)\)
Vậy trong A có 3 nguyên tố C, H, O.
b) Tỉ khối hơi của A so với hiđro là 23 nên:
Công thức phân tử của A là MA = 23 . 2 = 46.
Đặt công thức phân tử của A: CxHyOz.
Ta có tỉ lệ:
\(\begin{array}{l}
x:y:z = \frac{{{m_C}}}{{12}}:\frac{{{m_H}}}{1}:\frac{{{m_O}}}{{16}}\\
= \frac{{12}}{{12}}:\frac{3}{1}:\frac{8}{{16}}\\
= 1:3:0,5 = 2:6:1
\end{array}\)
Công thức của A có dạng (C2H6O)n
MA = 46 → n = 1.
Vậy công thức phân tử của A là C2H6O.
3. Luyện tập
3.1. Bài tập tự luận
Câu 1: Chỉ dùng H2O và một hoá chất, hãy phân biệt các chất sau: Rượu etylic, axit axetic, benzen.
Câu 2: Nêu hai phương pháp hóa học khác nhau để phân biệt hai dung dịch C2H5OH và CH3COOH
Câu 3: Tính khối lượng dung dịch axit axetic thu được khi lên men 5 lít rượu 400. Biết khối lượng riêng của rượu etylic là 0,8 g/ml và hiệu suất của quá trình lên men là 92%.
Câu 4: Giấm ăn được điều chế bằng cách lên men dung dịch rượu etylic ở nồng độ thấp. Hãy tính khối lượng giấm ăn 5% thu được khi lên men 50 lít rượu etylic 4°. Biết hiệu suất của quá trình lên men là 80%.
Câu 5: Hỗn hợp X gồm axit axetic và một axit hữu cơ có công thức CnH2n+1COOH. Tỉ lệ số mol tương ứng của hai axit là 1 : 2. Cho a gam hỗn hợp hai axit tác dụng vừa đủ với 300 ml dung dịch NaOH 1M rồi cô cạn thì thu được 27,4 gam hỗn hợp hai muối khan.
a) Hãy viết các phương trình hoá học của phản ứng xảy ra.
b) Xác định công thức phân tử của axit.
c) Tính thành phần phần trăm khối lượng của mỗi axit trong hỗn hợp.
3.2. Bài tập trắc nghiệm
Câu 1: Rượu etylic và axit axetic đều tác dụng với:
A. Na2CO3.
B. NaOH.
C. NaCl.
D. Na.
Câu 2: Phương pháp lên men rượu etylic loãng dùng để điều chế
A. Etylen.
B. Axit axetic
C. Natri axetat
D. Etyl axetat
Câu 3: Cho sơ đồ phản ứng sau:
C2H4 → X → CH3COOH → CH3COOC2H5
A. CH4.
B. C6H6.
C. C2H2.
D. CH3CH2OH.
4. Kết luận
Sau bài học cần nắm nội dung sau:
- Mối liên hệ giữa các chất etilen, rượu etilic, axit axetic, và etylaxetat.
- Tính được hiệu suất quá trình lên men, este hóa và xác định công thức phân tử.
Tham khảo thêm
- doc Hoá học 9 Bài 44: Rượu etylic
- doc Hoá học 9 Bài 45: Axit axetic
- doc Hoá học 9 Bài 47: Chất béo
- doc Hoá học 9 Bài 48: Luyện tập Rượu etylic, axit axetic và chất béo
- doc Hoá học 9 Bài 49: Thực hành: Tính chất của rượu và axit
- doc Hoá học 9 Bài 50: Glucozơ
- doc Hoá học 9 Bài 51: Saccarozơ
- doc Hoá học 9 Bài 52: Tinh bột và xenlulozơ
- doc Hoá học 9 Bài 53: Protein
- doc Hoá học 9 Bài 54: Polime
- doc Hoá học 9 Bài 55: Thực hành: Tính chất của gluxit
- doc Hoá học 9 Bài 56: Ôn tập cuối năm
