Hoá học 9 Bài 30: Silic và công nghiệp silicat
Silic là nguyên tố phổ biến thứ hai trong vỏ trái đất, ngành công nghiệp liên quan đến silic và hợp chất của nó gọi là công nghiệp silicat rất gần gũi trong đời sống, chúng ta hãy nghiên cứu về silic và ngành công nghiệp này.
Mục lục nội dung

1. Tóm tắt lý thuyết
1.1. Silic
Kí hiệu hóa học: Si
Nguyên tử khối: 28
a. Tính chất vật lí
- Trạng thái tự nhiên: Silic là chất rắn, màu xám, khó nóng chảy,có vẽ sáng của kim loại, dẫn điện kém, tinh thể silic tinh khiết là chất bán dẫn.
- Tính chất:
- Silic là phi kim hoạt động hoá học yếu hơn C, Cl2
- Silic tác dụng với oxi ở nhiệt độ cao: Si + O2
SiO2
- Silic để chế tạo pin mặt trời, dùng làm vật liệu bán dẫn trong kĩ thuật điện tử.
1.2. Silic đioxit
-
SiO2 là 1 oxit axit tác dụng với kiềm và oxit bazơ tạo thành muối silicat ở nhiệt độ cao
SiO2+NaOH .PNG)
SiO2+ CaO .PNG)
- SiO2 không phản ứng với nước
1.3. Công nghiệp silicat
a. Sản xuất đồ gốm sứ
- Nguyên liệu chính: Đất sét, thạch anh, fenpat.
- Các công đoạn chính
- Nhào đất sét, thach anh, và fenpat với nước rồi tạo hình, sấy khô.
- Nung các đồ vật trong lò ở nhiệt độ cao thích hợp.
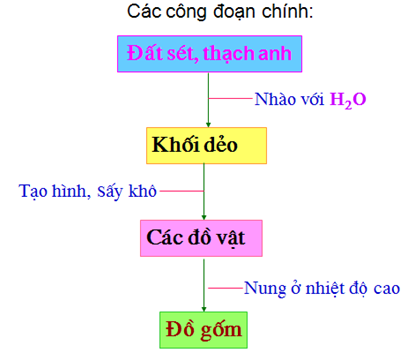
Cơ sở sản xuất: Gốm sứ bát tràng, Hải Dương, Đồng Nai.
b. Sản xuất xi măng
- Nguyên liệu chính: Đất sét, đá vôi, cát
- Các công đoạn chính:
- Nghiền nhỏ hỗn hợp thành dạng bùn.
- Nung hỗn hợp trên trong lò quay ở nhiệt độ 1400 → 15000C thu được clanhke rắn
- Nghiền clanhke nguội và phụ gia thành bột mịn đó là xi măng
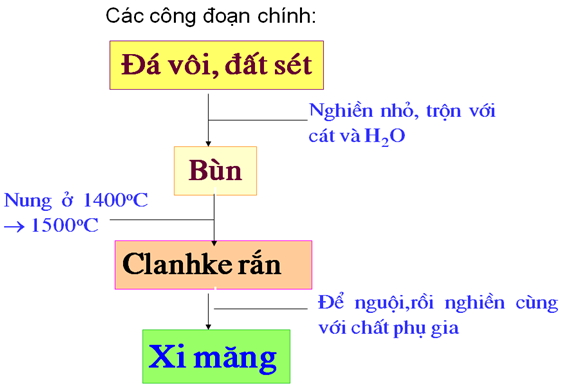
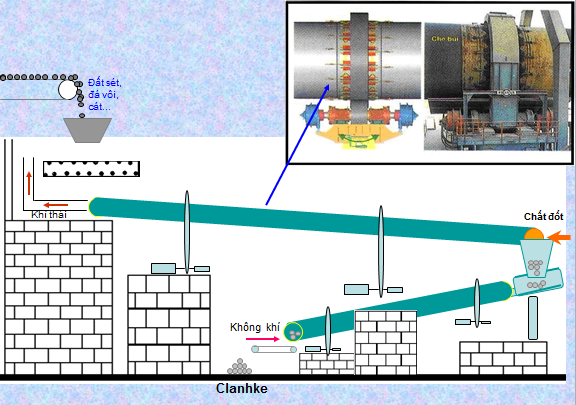
- Cơ sở sản xuất xi măng ở nước ta: Hải Dương, Thanh Hoá, Hải Phòng, Hà Nam
c. Sản xuất thuỷ tinh
- Nguyên liệu chính: Các thạch anh (cát trắng), đá vôi, sôđa (Na2CO3)
- Các công đoạn chính:
- Trộn hỗn hợp theo tỉ lệ thích hợp.
- Nung hỗn hợp khoảng 9000C
- Làm nguội từ từ được thuỷ tinh dẻo, ép thổi thuỷ tinh dẻo thành các đồ vật
- Các cơ sở sản xuất chính: Hải Phòng, Hà Nội, Đà Nẵng

2. Bài tập minh họa
2.1. Dạng 1: Phương trình hóa học
Viết các phương trình hoá học thực hiện những chuyển đổi hoá học sau:
1. Na2CO3 + ... → ... + ...
2. ... + SiO2 → ... + ...
Hướng dẫn giải
1. Na2CO3 + SiO2 → Na2SiO3 + CO2
2. CaCO3 + SiO2 → CaSiO3 + CO2
2.2. Dạng 2: Xác định công thức
Một loại thuỷ tinh dùng để làm cửa kính, hoặc đồ dùng gia đình có thành phần: 75% SiO2 ; 12% CaO ; 13% Na2O. Hãy tìm công thức hoá học của thuỷ tinh dưới dạng các oxit.
Hướng dẫn giải
Đặt công thức hóa học của loại thủy tinh này là: xNa2O.yCaO.zSiO2 (Với những điều kiện như sau : x, y, z là những số nguyên, dương)
Ta có: MNa2O = 62g; MCaO = 56g; MSiO2 = 60g
Tỉ lệ x : y : z là những số nguyên đơn giản nhất.
Theo đầu bài ta có tí lệ :
x : y : z = 13/62 : 12/56 : 75/60 = 0,21 : 0,21 : 1,25 = 1 : 1 : 6
Vậy công thức hóa học của loại thủy tinh trên là: Na2O.CaO.6SiO2
3. Luyện tập
3.1. Bài tập tự luận
Câu 1: Sản xuất thủy tinh như thế nào? Viết các phương trình phản ứng hóa học xảy ra trong quá trình nấu thủy tinh.
Câu 2: Những cặp chất nào dưới đây có thể tác dụng với nhau ? Viết các phương trình hoá học (nếu có).
a) SiO2 và CO2
b) SiO2 và NaOH
c) SiO2 và CaO
d) SiO2 và H2SO4
e) SiO2 và H2O
Câu 3: Thành phần chính của xi măng là gì? Cho biết nguyên liệu chính và mô tả sơ lược các công đoạn sản xuất xi măng.
3.2. Bài tập trắc nghiệm
Câu 1: Trong tự nhiên silic tồn tại ở dạng
A. Đơn chất.
B. Hợp chất
C. Hỗn hợp
D. Vừa đơn chất vừa hợp chất
Câu 2: Nguyên liệu để sản xuất đồ gốm là:
A. Đất sét, thạch anh, Fenfat.
B. Đất sét, đá vôi ,cát.
C. cát thạch anh, đá vôi, sođa.
D. Đất sét, thạch anh, đá vôi.
Câu 3: Silic ddioxxit là một oxit axit vì phản ứng với:
A. Nước và kiềm.
B. Nước và oxit bazơ.
C. Kiềm và oxit bazơ.
D. Kiềm và oxit axit.
4. Kết luận
Sau bài học cần nắm:
- Thông tin về silic, silic đioxit, muối silicat, sản xuất thuỷ tinh, đồ gốm, xi măng.
- Viết được các phương trình hóa học minh hoạ cho tính chất của Si, SiO2, muối silicat.
Tham khảo thêm
- doc Hoá học 9 Bài 25: Tính chất của phi kim
- doc Hóa học 9 Bài 26: Clo
- doc Hóa học 9 Bài 27: Cacbon
- doc Hoá học 9 Bài 28: Các oxit của cacbon
- doc Hoá học 9 Bài 29: Axit cacbonic và muối cacbonat
- doc Hoá học 9 Bài 31: Sơ lược về bảng tuần hoàn các nguyên tố hóa học
- doc Hoá học 9 Bài 32: Luyện tập chương 3
- doc Hoá học 9 Bài 33: Thực hành: Tính chất hóa học của phi kim và hợp chất của chúng
