Giải bài tập SBT Hóa 11 Bài 44: Anđehit - Xeton
Lời giải chi tiết và chính xác cho 12 bài tập trang 66,67 SBT Hóa lớp 11 đã được eLib sưu tầm và tổng hợp dưới đây sẽ giúp các em học tập thật tốt chuyên đề Anđehit - Xeton. Mời các bạn tải về tham khảo chuẩn bị cho bài học sắp tới.
Mục lục nội dung
1. Giải bài 9.1 trang 66 SBT Hóa học 11
2. Giải bài 9.2 trang 66 SBT Hóa học 11
3. Giải bài 9.3 trang 66 SBT Hóa học 11
4. Giải bài 9.4 trang 66 SBT Hóa học 11
5. Giải bài 9.5 trang 66 SBT Hóa học 11
6. Giải bài 9.6 trang 67 SBT Hóa học 11
7. Giải bài 9.7 trang 67 SBT Hóa học 11
8. Giải bài 9.8 trang 67 SBT Hóa học 11
9. Giải bài 9.9 trang 67 SBT Hóa học 11
10. Giải bài 9.10 trang 67 SBT Hóa học 11

Giải bài tập SBT Hóa 11 Bài 44: Anđehit - Xeton
1. Giải bài 9.1 trang 66 SBT Hóa học 11
Trong các chất có công thức cấu tạo ghi ở dưới đây, chất nào không phải là anđehit ?
A. H - CH = O
B. O = CH - CH = O
C. CH3 - CO - CH3
D. CH3 - CH = O
Phương pháp giải
Xem lại lí thuyết về Anđehit - Xeton
Anđehit là những hợp chất hữu cơ mà phân tử có nhóm CH= O liên kết trực tiếp với nguyên tử cacbon hoặc nguyên tử hiđro nên có công thức tổng quát là: R(CHO)n.
- Xeton là những hợp chất hữu cơ mà phân tử có nhóm –C=O- liên kết trực tiếp với hai gốc hiđrocacbon R và R' nên có công thức tổng quát là RCOR’
Hướng dẫn giải
CH3 - CO - CH3 là xeton
Đáp án C
2. Giải bài 9.2 trang 66 SBT Hóa học 11
Tên đúng của chất CH3 - CH2 - CH2 - CHO là:
A. propan-1-al
B. propanal
C. butan-1-al
D. butanal
Phương pháp giải
- Danh pháp thay thế: tên của hiđrocacbon tương ứng với mạch chính+ al
- Danh pháp thông thường: anđehit + tên axit tương ứng
Hướng dẫn giải
Tên đúng của chất CH3 - CH2 - CH2 - CHO là butanal.
Đáp án D
3. Giải bài 9.3 trang 66 SBT Hóa học 11
Anđehit propionic có công thức cấu tạo nào trong số các công thức dưới đây?
A. CH3 - CH2 - CH2 - CHO.
B. CH3 - CH2 - CHO.
C. CH3-CH(CH3)-CHO
D. HCOOCH2CH3
Phương pháp giải
- Danh pháp thông thường: anđehit + tên axit tương ứng
Hướng dẫn giải
Anđehit propionic có công thức cấu tạo là CH3 - CH2 - CHO
Đáp án B
4. Giải bài 9.4 trang 66 SBT Hóa học 11
Chất CH3-CH2-CH2-CO-CH3 có tên là gì?
A. pentan-4-on.
B. pentan-4-ol.
C. pentan-2-on.
D. pentan-2-ol.
Phương pháp giải
Xem lại lí thuyết về Anđehit - Xeton
- Tên thay thế = Tên HC tương ứng + on
- Tên gốc - chức = Tên gốc hydrocacbon + xêtôn
Hướng dẫn giải
Chất CH3-CH2-CH2-CO-CH3 có tên là pentan-2-on.
Đáp án C
5. Giải bài 9.5 trang 66 SBT Hóa học 11
Nhận xét nào sau đây là đúng?
A. Anđehit và xeton đều làm mất màu nước brọm.
B. Anđehit và xeton đều không làm mất màu nước brom.
C. Xeton làm mất màu nước brom còn anđehit thì không.
D. Anđehit làm mất màu nước brom còn xeton thì không.
Phương pháp giải
Xem lại lí thuyết về Anđehit - Xeton
Cấu trúc: Anđehit, xeton đều có nhóm – CO- gọi là nhóm cacbonyl trong phân tử.
Liên kết đôi C=O gồm một liên kết δ và một liên kết π kém bền hơn, tương tự liên kết đôi C=C trong phân tử anken
Hướng dẫn giải
Anđehit làm mất màu nước brom còn xeton thì không.
Đáp án D
6. Giải bài 9.6 trang 67 SBT Hóa học 11
Phản ứng CH3-CH2-OH + CuO → CH3-CHO + Cu + H2O thuộc loại phản ứng nào cho dưới đây ?
A. Phản ứng thế.
B. Phản ứng cộng.
C. Phản ứng tách.
D. Không thuộc cả 3 loại phản ứng đó.
Phương pháp giải
Phản ứng tách:
R(CH2OH)x + xCuO → R(CHO)x + xCu + xH2O
Hướng dẫn giải
Phản ứng CH3-CH2-OH + CuO → CH3-CHO + Cu + H2O thuộc loại phản ứng tách.
Đáp án C
7. Giải bài 9.7 trang 67 SBT Hóa học 11
Anđehit benzoic C6H5-CHO tác dụng với kiềm đậm đặc theo phương trình hoá học sau :
2C6H5CHO (anđehit benzoic) + KOH → C6H5COOK (kali benzoat) + C6H5CH2OH (ancol benzylic)
Trong phản ứng này thì
A. anđehit benzoic chỉ bị oxi hoá.
B. anđehit benzoic chỉ bị khử.
C. anđehit benzoic không bị oxi hoá, không bị khử.
D. anđehit benzoic vừa bị oxi hoá, vừa bị khử.
Phương pháp giải
Xác định số oxi hóa của nguyên tố trước và sau phản ứng → Kết luận.
Hướng dẫn giải
2C6H5CHO (anđehit benzoic) + KOH → C6H5COOK (kali benzoat) + C6H5CH2OH (ancol benzylic) trong phản ứng này thì anđehit benzoic vừa bị oxi hoá, vừa bị khử.
Đáp án D
8. Giải bài 9.8 trang 67 SBT Hóa học 11
Viết công thức cấu tạo và tên tất cả các anđehit và các xeton có cùng công thức phân tử C5H10O.
Phương pháp giải
- Anđehit:
Tên thay thế = Tên HC mạch chính + al
- Xeton:
+ Tên thay thế = Tên HC tương ứng + on
+ Tên gốc - chức = Tên gốc hydrocacbon + xêton
Hướng dẫn giải
Các anđehit:
CH3 - CH2 - CH2 - CH2 - CHO (pentanal)
CH3 - CH2 - CH(CH3) - CHO (2-metylbutanal)
CH3 - CH(CH3) - CH2 - CHO (3-metylbutanal)
CH3 - C(CH3)2 - CHO (2,2-đimetylpropanal)
Các xeton:
CH3 - CH2 - CH2 - CO - CH3 (pentan-2-on)
CH3 - CH2 - CO - CH2 - CH3 (pentan-3-on)
CH3 - CH(CH3) - CO - CH3 (3-metylbutan-2-ol)
9. Giải bài 9.9 trang 67 SBT Hóa học 11
Viết các phương trình hoá học của quá trình điều chế anđehit axetic xuất phát từ mỗi hiđrocacbon sau đây:
1. axetilen
2. etilen
3. etan
4. metan
Phương pháp giải
Học sinh tổng hợp kiến thức về các hợp chất có liên quan để viết PTHH.
Hướng dẫn giải
1. CH ≡ CH + H2O → CH3-CHO (đk: HgSO4, 80oC)
2. 2CH2 = CH2 + O2 (to, xt) → 2CH3 − CHO
3. CH3 − CH3 → CH2 = CH2 + H2 (đk: 150oC, xt)
2CH2 = CH2 + O2 (to, xt) → 2CH3 − CHO
4. 2CH4 → CH ≡ CH + 3H2 (đk:1500oC
CH ≡ CH + H2O → CH3-CHO (đk: HgSO4, 80oC)
10. Giải bài 9.10 trang 67 SBT Hóa học 11
Chất A là một anđehit đơn chức. Cho 10,50g A tham gia hết vào phản ứng tráng bạc. Lượng bạc tạo thành được hoà tan hết vào axit nitric loãng làm thoát ra 3,85 lít khí NO (đo ở 27,3oC và 0,80 atm). Xác định công thức phân tử, công thức cấu tạo và tên chất A.
Phương pháp giải
- Đổi thể tích khí NO về đktc theo công thức: Vo=pVT.TopoVo=pVT.Topo
- Viết PTHH:
R - CHO + 2AgNO3 + 3NH3 + H2O → RCOONH4 + 2NH4NO3 + 2Ag
3Ag + 4HNO3 → 3AgNO3 + NO + 2H2O
- Tính theo PTHH → R
- Viết CTCT và gọi tên A.
Hướng dẫn giải
Đổi thể tích khí NO về đktc :
Vo=pVT.Topo=0,8.3,85300,3.2731=2,8(l)Vo=pVT.Topo=0,8.3,85300,3.2731=2,8(l)
R - CHO + 2AgNO3 + 3NH3 + H2O → RCOONH4 + 2NH4NO3 + 2Ag
3Ag + 4HNO3 → 3AgNO3 + NO + 2H2O
Số mol Ag = 3.số mol NO = 3.2,822,42,822,4 = 3,75.10−13,75.10−1 (mol).
Số mol RCHO = 1212Số mol Ag = 3,75.10−123,75.10−12 .
Khối lượng của 1 mol RCHO = 10,5.23,75.10−110,5.23,75.10−1 = 56 (g).
RCHO = 56 → R = 56 - 29 = 27 → R là -C2H3
CTPT là C3H4O.
CTCT là CH2 = CH - CHO (propenal).
11. Giải bài 9.11 trang 67 SBT Hóa học 11
Để đốt cháy hoàn toàn một lượng chất hữu cơ A phải dùng vừa hết 3,08 lít O2. Sản phẩm thu được chỉ gồm có 1,80 g H2O và 2,24 lít CO2. Các thể tích khí đo ở đktc.
1. Xác định công thức đơn giản nhất của A.
2. Xác định công thức phân tử của A, biết rằng tỉ khối hơi của A đối với oxi là 2,25.
3. Xác định công thức cấu tạo có thể có của chất A, ghi tên tương ứng, biết rằng A là hợp chất cacbonyl.
Phương pháp giải
1. Áp dụng ĐLBTKL, tính mA=mCO2+mH2O−mO2mA=mCO2+mH2O−mO2
- Tính khối lượng C, H, O có trong A.
- Lập tỉ lệ các nguyên tố C, H, O → CTĐGN
2. Tính phân tử khối của A dựa vào tỉ khối hơi
3. Viết CTCT và gọi tên A.
Hướng dẫn giải
1. Theo định luật bảo toàn khối lượng :
mA=mCO2+mH2O−mO2=2,2422,4.44+1,8−3,0822,4.32mA=mCO2+mH2O−mO2=2,2422,4.44+1,8−3,0822,4.32 = 1,8 (g)
Khối lượng C trong 1,8 g A là : 12.2,2422,412.2,2422,4 = 1,2 (g).
Khối lượng H trong 1,8 g A là : 2.1,8182.1,818 = 0,2 (g).
Khối lượng O trong 1,8 g A là : 1,8 - 1,2 - 0,2 = 0,4 (g).
Công thức chất A có dạng CxHyOz :
x : y : z = 1,212:0,21:0,4161,212:0,21:0,416 = 0,1 : 0,2 : 0,025 = 4:8:1
CTĐGN là C4H8O
2. MA = 2,25.32 = 72 (g/mol)
→ CTPT trùng với CTĐGN : C4H8O.
3. Các hợp chất cacbonyl C4H8O :
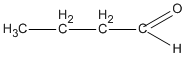 (butanal)
(butanal)
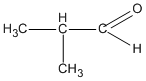 (2-metylpropanal )
(2-metylpropanal )
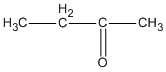 (butan-2-ol )
(butan-2-ol )
12. Giải bài 9.12 trang 68 SBT Hóa học 11
Hỗn hợp M chứa ba chất hữu cơ A, B và C là 3 đồng phân của nhau. A là anđehit đơn chức, B là xeton và C là ancol. Đốt cháy hoàn toàn 1,45 g hỗn hợp M, thu được 1,68 lít khí CO2 (đktc) và 1,35 g H2O. Hãy xác định công thức phân tử, công thức cấu tạo và tên của A, B và C.
Phương pháp giải
- A, B và C có công thức phân tử CxHyO
- Viết PTHH: CxHyO+(x+y4−12)O2→xCO2+y2H2OCxHyO+(x+y4−12)O2→xCO2+y2H2O
- Dựa vào dữ kiện đề bài và PTHH → x, y → CTPT.
- Viết CTCT của A, B, C.
Hướng dẫn giải
Ba chất A, B, C là đồng phân nên có CTPT giống nhau. A là anđehit đơn chức nên phân tử A chỉ có 1 nguyên tử oxi. Vậy A, B và C có công thức phân tử CxHyO. Khi đốt cháy hoàn toàn hỗn hợp M :
CxHyO+(x+y4−12)O2→xCO2+y2H2OCxHyO+(x+y4−12)O2→xCO2+y2H2O
Theo phương trình : (12x + y + 16) g M tạo ra x mol CO2 và y2y2 mol H2OH2O
Theo đầu bài : 1,45 g M tạo ra 1,6822,41,6822,4 mol CO2 và 1,35181,3518 mol H2OH2O
12x+y+161,45=x0,075=y0,1512x+y+161,45=x0,075=y0,15
→ x = 3 ; y = 6.
CTPT của A, B và C là C3H6O.
A là 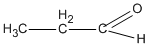 (propanal)
(propanal)
B là 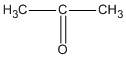 (propanon hay axeton) ;
(propanon hay axeton) ;
C là CH2 = CH - CH2 - OH (propenol).

